Влияние Реосорбилакта на регионарную гемодинамику у больных хронической критической ишемией нижних конечностей и мультифокальным атеросклерозом
НМУ им. акад. А.А. Богомольца, кафедра госпитальной хирургии №2
Резюме. Обработаны статистические данные о летальности и ее причинах среди 844 пациентов ХКИНК, оперированных в городском центре хирургии г. Киева за период с 1997 по 2005 гг. Изучено 90 пациентов с односторонними поражениями артериального русла конечности дистальнее уровня паховой связки, разделенных на три равнозначные группы по 30 человек, выделенных в зависимости от стадии ишемии.
Всем им в схему терапии был включен инфузионный препарат Реосорбилакт. Контрольную группу составили 90 равнозначных больных, которым применяли общепринятую схему лечения без использования Реосорбилакта. Предметом изучения было: интенсивность болевого синдрома, выраженность отека, проходимость, а также скорость и величина регионального давления на уровне подколенной и задней большеберцовой вен в пораженной и контрлатеральной конечностях с расчетом артерио-венозных градиентов, давления в стволе легочной артерии (ЛА), динамика насыщенности периферической венозной и артериальной крови кислородом, качественные показатели тромбообразования, а также морфологические характеристики вен конечностей и легочной ткани. Полученные данные аргументируют использование Реосорбилакта для лечения больных с ХКИНК, что может в значительной степени улучшить региональный кровоток и уменьшить риск венозных осложнений.
Ключевые слова: хроническая критическая ишемия нижних конечностей, венозный тромбоз, ле- гочные осложнения, патогенез, Реосорбилакт.
Известно, что артериальное и венозное кровообращение в нижних конечностях находятся в тесном взаимодействии. Так, по данным В. Г. Харченко (1970), при варикозной болезни развиваются изменения артериального кровообращения в результате нарушений венозного оттока. При этом артерии не только больной, но и здоровой конечности реагируют спазмом, который носит рефлекторный характер и ведет к уменьшению поступления крови в дистальные отделы конечности [4]. В связи с этим можно предположить, что противоположный эффект возможен при хронической критической ишемии нижних конечностей (ХКИНК). В то же время при ХКИНК выявляется смешанная форма гипоксии, включающая в себя гемическую — низкое насыщение гемоглобина кислородом, гипоксическую — снижение рО2 в артериальной крови, тканевую — снижение утилизации кислорода тканями (5,8). Исследования в этом направлении представляют несомненный интерес, поскольку смешанная гипоксия, которая, по сути, определяет тяжесть течения облитерирующих заболеваний артерий, способствует возникновению грубых нарушений обменных процессов . Последнее позволяет полагать, что биохимические параметры регионарной крови, отражающие состояние метаболизма в ишемизированной конечности, могут служить критериями тяжести и прогноза облитерирующих заболеваний артерий. Анализ данных отечественной и зарубежной литературы в этом вопросе привел нас к заключению о недостаточной изученности центральной и периферической венозной гемодинамики у больных ХКИНК. Нет единого мнения о патогенетических механизмах в цепочке: регионарная ишемия — нарушения периферической венозной гемодинамики — циркуляторная гипоксия — регионарная ишемия. Несмотря на большое количество легочных осложнений в хирургии ХКИНК современная литература не предоставила однозначных данных о причинно-следственных связях между усугублением тяжести основного заболевания, изменениями в легочной гемодинамике и вентиляционными осложнениями. Не изучено также влияние Реосорбилакта на регионарную гемодинамику у больных хронической критической ишемией нижних конечностей и мультифокальным атеросклерозом.
Цель работы
Изучить состояние регионарной и венозной гемодинамики, морфологические изменения в сосудах нижних конечностей и легочной ткани, а также выработать меры профилактики венозных осложнений в хирургии ХКИНК.
Материалы и методы
Обработаны статистические данные о летальности и их причинах среди 844 пациентов ХКИНК, оперированных в городском центре хирургии г. Киева за период с 1997 по 2005 г.г. Результаты анализа показали, что госпитальная летальность составила 2,7% (23 б-х). Анализ причин летальности показал, что у 3-х больных была выявлена ТЭЛА, у 2-х–пневмония с наличием множественных микроинфарктов в легочной ткани. У всех 5-ти пациентов длительность критической ишемии превышала 7 недель, длительность отека конечности — 3 недели, при морфологическом исследовании у них были выявлены свежие венозные тромбозы в берцовых и мышечных венах пораженных конечностей. Таким образом, можно предположить, что в структуре причин смертности больных ХКИНК 21,7% занимают венозные осложнения.
В группу изучения вошли 90 пациентов с односторонними поражениями артериального русла конечности дистальнее уровня паховой связки, разделенных на 3 равнозначных группы по 30 человек, выделенных в зависимости от стадии ишемии: III-A, III-Б и IV. Всем им, вне зависимости от стадии ишемии, в лечебную программу был включён инфузионный препарат Реосорбилакт. Контрольную группу составили 90 аналогичных пациентов, которым Реосорбилакт не вводился. Группы больных существенно не отличались по признакам пола, возраста, расы и социального положения. Предметом изучения были следующие показатели: интенсивность болевого синдрома, выраженность отека, величина субфасциального давления, проходимость, а также скорость и величина регионарного давления на уровне подколенной и задней большеберцовой вен в пораженной и контралатеральной конечностях с расcчетом артерио-венозных градиентов, давление в стволе легочной артерии (ЛА), динамика насыщенности периферической венозной и артериальной крови кислородом, качественные показатели тромбообразования, продолжительность венозной фазы после артериографии, клинические и рентгенологические критерии легочного воспаления, а также морфологические характеристики венозной и легочной ткани.
Характеристики центрального и регионарного кровотока изучали с использованием УЗД аппаратов «Power Vision» фирмы “Toshiba” и “Aloka-5000” (Япония), спирального КТ-томографа “Volume ZOOM” фирмы «Siemens» (Германия), ангиографа “Integris – 3000” фирмы “Philips” (Нидерланды), газовый состав крови определяли при помощи газового анализатора на аппарате «Super- 818» фирмы «Mitsubishi» (Япония), тромбообразование в системе периферических вен изучали методом определения Д-димера, морфологию тканей изучали методом «ОКГ» по Зербино Д.Д., интенсивность болевого синдрома отмечали сами больные при помощи специальных шкал боли, субфасциальное давление в пораженной конечности определяли при помощи одноразовых аппаратов Вальдмана, объем конечности замеряли по методу В.Г. Мишалова и соавт.
РЕЗУЛЬТАТЫ
Регионарный кровоток
Анализ результатов измерения регионарного систолического давления (РСД) в пораженных конечностях показал их разницу в зависимости от применения в схеме лечения Реосорбилакта (рис.1).
В контралатеральной конечности, не пораженной атеросклеротическим процессом, несмотря на нормальные показатели в стадии III-А проявилась тенденция к достоверному снижению РСД и снижению полученного градиента при более тяжелых стадиях ишемии (рис.2).
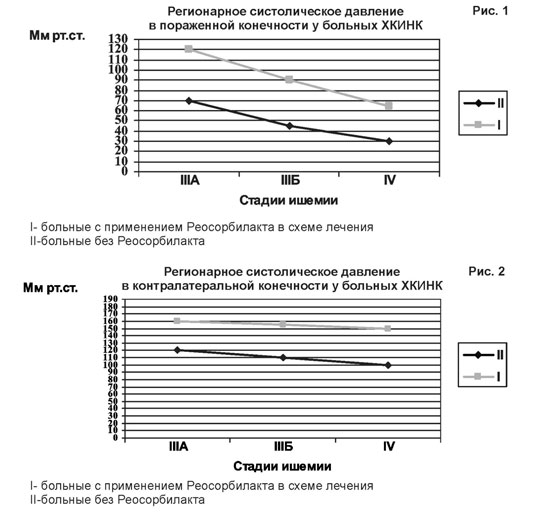
Параметры периферической венозной гемодинамики существенно отличались в зависимости от стадии ишемии, положения тела и точки замера. Так, в пораженных конечностях результаты измерения периферического венозного давления (ПВД) свидетельствовали о его неравномерном повышении по сравнению с нормальными величинами при всех стадиях ишемии, особенно у больных без использования Реосорбилакта. Динамика кривой ПВД в подколенной вене характеризовалась прогрессивным ростом цифр при отсутствии в схеме лечения Реосорбилака и ломаной кривой у пациентов с его применением. Последняя характеризовалась некоторым относительным снижением ПВД при III-Б стадии ишемии по отношению к III-А и ростом при IV стадии.
Венозная гемодинамика в контралатеральных конечностях, в отличие от артериальной, характеризовалась отсутствием патологических сдвигов как в первой, так и во второй группах. Таким образом, при прогрессировании ишемии у пациентов изучаемой группы в III-Б стадии происходило постепенное и достоверное снижение ПВД в пораженной конечности в горизонтальном положении (на 40,0 %) по отношению к стадии III-А, в контрольной, наоборот, отмечалась некоторая тенденция к повышению ПВД (на 9,1 %). Здесь, по-видимому, важное значение имел фактор экстравазального сдавления, усиленный ишемическим отеком (рис.3).
Показатели ПВД на уровне заднебольшеберцовой вены были несколько иными, чем в подколенной, особенно в III-Б стадии (рис.4).
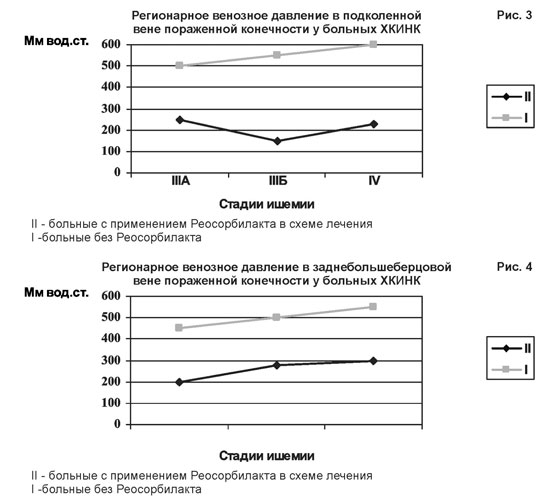
Снижалась также и линейная скорость кровотока по подколенной и заднебольшеберцовой венам в пораженных конечностях, составляя в среднем при III-А стадии 46,7% от нормы, при III-Б стадии 31,8% и в IV стадии 24 %. Следует отметить,что при III-Б стадии были получены неоднозначные данные по линейной скорости кровотока в подколенной и заднебольшеберцовой венам, а именно, некоторое относительное повышение в подколенной и резкое снижение в заднебольшеберцовой.
При оценке артериовенозного индекса существенной разницы между нормой и III-А стадией выявлено не было (артерио-венозный индекс у больных в группе изучения составил 2,8, в контрольной -2,4). В стадии III-Б он почти не изменился в группе изучения 3,0 и был существенно ниже в контрольной 1,6, в IV стадии он был значительно ниже — соответственно -1,6 и 1,1. Можно также отметить практически полное совпадение величин этого индекса в группе изучения и в контрольной для каждой из стадий ишемии (Табл.1).
|
Таблицa 1 Показатели гемодинамических индексов на стороне поражения у больных ХКИНК |
|||||
| Стадия ишемии | А/В | А/А | В/В(подк.) | В/В(ЗББВ) | |
| Гр.1 лакта | Гр.2 | стоя/лежа | стоя/лежа | стоя/лежа | |
| III-А | 2,8±0,3 | 2,4 ± 0,3 | 1,7 ± 0,1 | 2,0± 0,2* | 2,25± 0,2* |
| III-Б | 3,0±0,4* | 1,6 ±0,1* | 2,0 ±0,2* | 3,7± 0,3* | 1,8± 0,2* |
| IV | 1,6±0,2 | 1,1±0,1 | 2,2 ±0,2* | 2,6± 0,2* | 1,8± 0,2* |
| Примечание: А/В — артерио-венозный индекс, А/А — отношение АД в положении стоя к АД в положении лежа, В/В — отношение ПВД в положении стоя к ПВД в положении лежа. *- р < 0,05. | |||||
Насыщенность артериальной и венозной крови кислородом
В центральном кровотоке нормальным показателем рО2 в артериальной крови является 100 мм.рт.ст., в венозной – 40 мм.рт.ст. Полученные результаты измерения рО2 представлены на рис. 5.
Давление в легочной артерии
При изучении показателей гемодинамики в ЛА больные были условно разделены на 2 группы: А — с клиническими признаками тромбоза вен по- раженной конечности, Б — без таковых. Группу А составили 12 пациентов: при III-А стадии – 0, при III-Б – 5, при IV стадии- 7. Группу Б составили 78 пациентов, соответственно при III-А стадии – 30, при III-Б– 25, при IV стадии– 23. Показатели си- столического давления в ЛА у этих больных представлены на рис. 6.
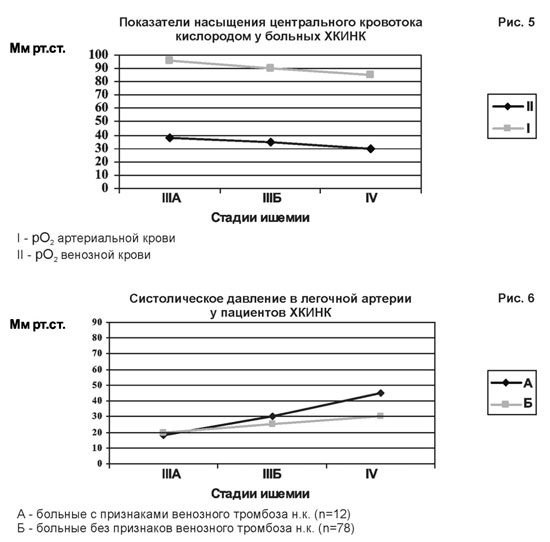
Анализ показателей систолического давления в ЛА у больных ХКИНК выявил следующие закономерности: достоверное повышение СДЛА у больных с III-Б стадией ишемии по отношению к III-А на 40% среди больных группы А и соответственно на 20% у больных группы Б. При IV ст. ишемии эти данные были следующими: 60% и 33%.
Выраженность болевого синдрома
Боли покоя фиксировались пациентами самостоятельно ежедневно в одно и то же время суток на протяжении всего времени пребывания в стационаре на специальных 100-мм шкалах. Средние величины болевых ощущений были следующими: для III-А стадии — 20 ± 3, III-Б стадии — 35 ± 4, для IV стадии — 70 ± 6. В группе пациентов, которым вводили Реосорбилакт по стандартной схеме средние величины боли уменьшились на 6 ± 1.
Показатели Д-димера
Определение Д-димера в крови проводили с помощью набора Roche/Diagnostika Stago; в основе метода лежит агглютинация латексных частиц, покрытых моноклональными антителами к Д-димеру. Суть метода состоит в возникновении агглютинации частиц латекса в течении 3 мин. при наличии в исследуемом образце крови Д-димера в концентрации, превышающей 0,5 мкг/мл. В группе из 12 больных с подтвержден- ным диагнозом острый венозный тромбоз проба на наличие Д-димера была положительной у 11(91,7%) и отрицательной у 1(8,3%) человек. Среди 78 больных, у которых диагноз острый венозный тромбоз не был подтвержден клинически, проба на наличие Д-димера была отрицательной у 59 (75,6 %) и положительной у 19 (24,4%) больных. Таким образом, при чувствительности теста на Д-димер в 96%, и специфичности в 82% можно предположить о наличии в исследуемых группах пациентов с III-Б и IV стадиями ишемии нижних конечностей 6 % ранее не диагностированных случаев периферических венозных тромбозов в пораженных и, возможно, контралатеральных конечностях.
Среди больных группы изучения (Реосорбилакт) было отмечено снижение показателей Д–димера до отрицательных у 91,7 %.
Выраженность отека конечности
Объем конечностей рассчитывали по специальной формуле, используя закон усеченного конуса:
Vk = 0,027
[ h1.(l12 + l1.l2 + l22) + h2.(l32 + l3.l4 + l42) + h3.(l42 + l4.l5 + l52)]
Где: Vk – объем конечности,
l1 — окружность верхней трети бедра,
l2 — окружность нижней трети бедра,
l3 — окружность верхней трети голени,
l4 — окружность средней трети голени,
l5 — окружность нижней трети голени,
h1— высота бедра,
h2 — высота от верхней трети голени до ее средней трети,
h3 — высота от средней трети голени до ее нижней трети.
Измерениям подлежали как пораженные, так и контралатеральные конечности с математическим рассчетом разницы их объемов. Данные замеров показали прямую зависимость между величиной отека, степенью ишемии пораженной конечности, а также использованием в схемах лечения больных Реосорбилакта. Контралатеральная сторона существенно не реагировала на ишемию и изменения схем лечения.
Морфологические исследования
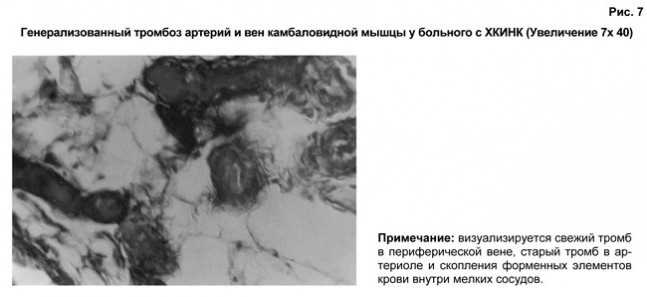
При морфологическом изучении тканей ишемизированных конечностей были выявлены кроме облитераций артериальных сосудов множественные утолщения стенок венул, обусловленные пролиферацией эндотелия и плазматическим их пропитыванием с проникновением фибрина в просвет венозных сосудов (рис.7). Последние были тромбированы на уровне стоп и нижних третей голеней в 98% исследуемых образцов тканей. В легочной ткани выявлены свежие и старые тромбозы мелких ветвей ЛА (рис.8).

А. Реканализация легочной артерии диаметром около 175 мкм (толстая стрелка) и эксцентрический фиброз легочной артерии диаметром около 200 мкм (тонкая стрелка).
Б. тромбоз легочной артерии (стрелка).
Увеличение х 100. Окраска Verhoeff’s — Van Gieson.
Обсуждение
Особенностями системы кровообращения у больных (ХКИНК) являются: приспособительный характер артериальной гипертензии, ограничение резервов кровоснабжения органов и тканей, снижение венозного притока к сердцу, метаболическое повреждение органов-мишеней, отсутствие функциональных резервов регуляции сократимости миокарда и сердечного выброса (3). Перестройка центральной гемодинамики у больных ХКИНК выражается в увеличении ударного и минутного объёмов сердца, укорочении периода напряжения и удлинении периода изгнания. С возрастом суживаются возможности диапазона изменений работоспособности сердца, но в то же время возникают совершенно новые механизмы регулирования кровообращения, характеризующиеся своеобразием реакций сердечно- сосудистой системы (7). Ауторегуляция системной гемодинамики у лиц пожилого и старческого возраста существенно отличается от таковой у молодых пациентов. У пожилых имеет место объёмная регуляция поддержания ударного выброса, смещение регуляции артериального дав- ления в гуморально-метаболическую сторону (2).
У пожилых чаще наблюдается повышенное артериальное давление, урежение частоты пульса (9). По данным B.C. Савельева и В.М. Кошкина (1997) у больных ХКИНК атеросклеротического генеза нередко наблюдается патология со стороны органов дыхания (10). По данным F.A. Metsen et al. (1980) напряжение кислорода, регистрируемое методикой чрескожного измерения, коррелирует с рО2 артериальной крови и количественно характеризует кожный кровоток (11).
Таким образом, состояние периферической гемодинамики в ишемизированных нижних конечностях тесно связано с функционированием дыхательной системы. Возникающие респираторные нарушения во время реваскуляризирующей операции во многом зависят от методики предоперационной подготовки и выбора метода анестезии.
Таким образом, система кровообращения, микроциркуляции, дыхания и газообмена у больных критической ишемией нижних конечностей атеросклеротического генеза исходно депремированы и их функционирование тесно взаимосвязано. Неблагоприятное воздействие операционной травмы и общий наркоз на одну из систем в этой цепочке вызовет ещё большую декомпенсацию ишемизированных конечностей и организма в целом.
О важности изучения нарушений гемодинамики в комплексе с изменениями биохимических показателей крови утверждала Р.Н. Лебедева (1988).
По данным Я.Л. Вострикова (1988) у больных облитерирующим атеросклерозом при нарастании недостаточности кровообращения и гипоксии в тканях пораженных конечностей происходит прогрессивное нарушение метаболических процессов, доходящее до декомпенсированного метаболического ацидоза (1). Основными составляющими при этом являются: макро- и микроэмболизация (воздушная или материальная), диффузная гипоперфузия и системная воспалительная реакция. Данные процессы приводят к снижению тканевого кровотока, что, в свою очередь, запускает целый каскад патологических реакций. К ним относятся: энергетический дефицит, лактат-ацидоз, нарушение ионного транспорта, глутаматная «эксайтотоксичность», внутриклеточное накопление кальция, активация внутриклеточных ферментов. Затем наблюдаются отдаленные последствия ишемии (оксидантный стресс, микроциркуляторно-клеточные реакции), которые могут завершиться апоптозом клеток или некрозом тканей.
Признаками, подтверждающими развитие артериовенозного шунтирования крови при критической ишемии, являются артериализация венозной крови, взятой из пораженной конечности (снижение но сравнению с предыдущей стадией рСО2, и повышение рО2, практически до нормальных значений), а также появление paнней венозной фазы при рентгенконтрастной ангиографии. Причинами развития этого феномена служит резкое снижение тонуса артерий (что подтверждается почти полным отсутствием реакции на нитроглицерин при реовазографическом исследовании) на фоне сохраняющегося высокого периферического сопротивления, обусловленного гемореологическими расстройствами, в частности повышением вязкости крови на 7-12% (при разных скоростях сдвига), гематокрита (от 48,9% III-А стадии до 50,1% при критической ишемии) и индекса, жесткости эритроцитов (на 5,5%) по сравнению с предшествующей стадией ишемии. Определенную роль в повышении периферического сопротивления кровотоку играет прилипание эритроцитов к сосудистой стенке. Механизмом компенсации нарушения транскапиллярного обмена, связанного с высокой скоростью тока крови через артериоло-венулярные шунты, является повышение венозного давления в пораженной конечности (в 1,5 — 2,1 раза по сравнению с нормой в горизонтальном положении и в 4,3 — 5 раз — в вертикальном). При этом не только увеличивается время прохождения крови по микрошунтам, но и уменьшается ее объем, «сбрасываемый» по артериовенозным анастомозам.
Таким образом, прогрессирование хронической ишемии нижних конечностей сопровождается для горизонтального положения постепенным снижением регионарного артериального и венозного давления. Артериовенозный индекс также снижается за счет относительно большего уменьшения АД. При этом, если снижение АД может быть связано как с редукцией артериального кровотока, так и со снижением сосудистого тонуса, то прогрессирующее относительное снижение венозного давления можно объяснить только низким тонусом венозных сосудов.
Если стадия III-А значительно не отличается от стадии II-Б по периферической гемодинамике, а различаются они в основном клинически, т. е. наличием или отсутствием «боли покоя», то в стадии III-Б складывается совершенно другая гемодинамическая ситуация не только за счет больших количественных отличий от менее тяжелой ишемии, но и вследствие появления нового фактора, участвующего в гемодинамических реакциях, — ишемического отека тканей голени. Он в большой степени определяет как повышение АД в дистальных отделах пораженной конечности в ортостазе, значение чего очевидно, так и повышение в этом положении венозного давления. Последнее создает более благоприятные условия для транскапиллярного обмена за счет замедления кровотока по артериоловенулярным шунтам. Кроме того, снижается сброс крови по более крупным (артериовенозным) шунтам, что уменьшает «обкрадывание» дистальных отделов пораженной конечности.
Известно, что четыре из пяти тромбозов глубоких вен протекают бессимптомно. В связи с этим поиск оптимального алгоритма диагностики венозных тромбозов представляется актуальным. Раннее выявление признаков активации свертывания крови и внутрисосудистого фибринообразования может существенно повысить эффективность диагностики и профилактики тромботических осложнений у больных с ХКИНК. В последние годы наибольшее внимание уделяется изучению роли маркеров образования и плазминового расщепления фибрина, одним из которых является Д-димер. Д-димер — один из конечных продуктов плазминовой деградации стабилизированного фибрина — является специфичным маркером внутрисосудистых отложений фибрина. Повышение его концентрации в плазме отражает активацию внутрисосудистого свертывания крови. Использование этого метода в диагностическом алгоритме у больных ХКИНК позволяет выявлять клинически не проявляемые случаи венозных тромбозов.
Легочная гипертензия (ЛГ) — это состояние, являющееся возможным следствием целого ряда заболеваний или имеющее идиопатическую природу, которое характеризуется постепенным повышением легочного сосудистого сопротивления и давления в легочной артерии, что приводит к развитию правожелудочковой недостаточноcти и гибели пациентов. Диагноз ЛГ определяется при среднем давлении в легочной артерии более 25 мм рт. ст. в покое и более 50 мм. рт.ст. при физической нагрузке. Как показали наши исследования, ЛГ является маркером тяжелых форм течения ХКИНК.
Согласно последней классификации, принятой ВОЗ в 1998 г. все варианты ЛГ объединены в одну группу клинически схожих заболеваний, что позволяет клиницисту определить план обследования пациентов с ЛГ и тактику лечения (6). Мы считаем, что больные с ХКИНК должны занять определенное место в структуре данной классификации. В патогенезе ЛГ выделяют четыре основных патофизиологических феномена, сочетание которых раскрывает сущность процессов ремоделирования легочных сосудов: вазоконстрикция, редукция легочного сосудистого русла, снижение эластичности легочных сосудов, облитерация легочных сосудов (тромбоз in situ, пролиферация гладкомышечных клеток) (рис. 8).
У больных с ХКИНК возможны вторичные формы ЛГ, когда дисфункция или повреждение эндотелия возникают предположительно вследствие процессов, являющихся первопричиной самой патологии, таких как воздействие токсинов, лекарств, аутоиммунные поражения, отложение фибрина. Освобождение хемотаксическнх агентов из поврежденных клеток пораженной конечности вызывает миграцию гладкомышечных клеток в интиме легочных артериол. Дополнительно секреция локально активных медиаторов с выраженным вазоконстрикторным действием способствует развитию тромбоза in situ, трансформируя легочное сосудистое русло из обычного антикоагулянтного состояния (вследствие освобождения простациклина и ингибитора тканевого активатора плазминогена) в прокоагулянтное. В результате образуется порочный круг, когда повреждение эндотелия неуклонно прогрессирует и приводит к ремоделированию легочных сосудов, нарастанию сосудистой обструкции и облитерации.
Реосорбилакт обладает реологическим, противошоковым, дезинтоксикационным, действием. Основными фармакологически активными веществами препарата являются сорбитол и натрия лактат. Сорбитол быстро включается в общий метаболизм, 80-90% его утилизируется в печени и накапливается в виде гликогена, 5% откладывается в тканях мозга, сердечной мышце и скелетной мускулатуре, 6-12% — выделяется с мочой. В печени сорбитол сначала превращается в фруктозу, которая в дальнейшем превращается в глюкозу, а затем в гликоген. Часть сорбитола используется для срочных энергетических нужд, другая часть откладывается как запас в виде гликогена. Изотонический раствор сорбитола обладает дезагрегантным действием и, таким образом, улучшает микроциркуляцию и перфузию тканей.
При введении в сосудистое русло из натрия лактата высвобождается натрий, СО2 и Н2О, которые образовывают бикарбонат натрия, что приводит к увеличению щелочного резерва крови. В отличие от раствора бикарбоната, коррекция метаболического ацидоза с помощью натрия лактата проходит медленнее, по мере включения его в обмен веществ, не возникает резких колебаний рН. Активной считается только половина введенного натрия лактата (изомер L), а другая половина (изомер D) не метаболизируется и выделяется с мочой. Действие натрия лактата проявляется через 20-30 минут после введения.
Реосорбилакт применяют для уменьшения интоксикации, улучшения микроциркуляции, коррекции кислотно-щелочного состояния, улучшения гемодинамики при шоках, острой кровопотере, а также при при затяжных гнойных процессах, различных инфекционных заболеваниях, предоперационной подготовке и в послеоперационном периоде, при тромбооблитерирующих заболеваниях кровеносных сосудов.
Реосорбилакт вводят внутривенно струйно или капельно:
• при травматическом, ожоговом, послеоперационном и гемолитическом шоках по 600-1000 мл (10-15 мл/кг массы тела больного) однократно и повторно, сначала струйно затем капельным методом;
• при хронических гепатитах по 400 мл (6-7 мл/кг массы тела) капельно, повторно;
• при острой кровопотере по 1500-1800 мл (до 25 мл/кг массы тела). В этом случае инфузию реосорбилакта рекомендуется проводить на догоспитальном этапе в специализированной машине скорой помощи;
• в предоперационном периоде и после различ- ных хирургических вмешательств в дозе 400 мл (6-7 мл/кг массы тела) капельно, однократ- но и повторно, ежедневно на протяжении 3-5 дней;
• при тромбооблитерирующих заболеваниях кровеносных сосудов из расчета 8-10 мл/кг массы тела капельно повторно через день. На курс лечения 10 инфузий.
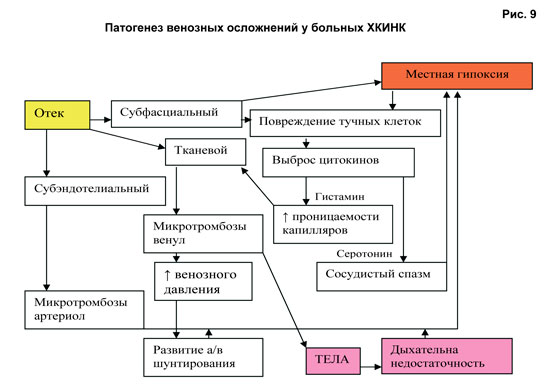
Таким образом венозную фазу патогенеза ХКИНК можно представить следующим образом (рис. 9):
Выводы:
1. Нарушения периферической венозной гемодинамики являются важной составляющей в патогенезе ХКИНК.
2. Вследствие ишемического отека, пареза сосудов, артерио-венозного шунтирования и местного воспаления у больных тяжелыми формами ХКИНК возникает венозный тромбоз в сосудах пораженной голени и стопы.
3. Венозный тромбоз при ХКИНК приводит к развитию перманентной ТЭЛА мелких ветвей и дыхательной недостаточности.
4. Развившаяся дыхательная гипоксия, сочетаясь с гемической, циркуляторной и тканевой усугубляет клинику ХКИНК и прогноз заболевания.
5. Использование Реосорбилакта для лечения больных с ХКИНК может в значительной степени уменьшить риск венозных осложнений.