Современные подходы к коррекции гемодинамических нарушений у больных с тяжелой сочетанной травмой
Обоснование. Выбор рациональной программы инфузионной терапии при тяжелой травме остается актуальной проблемой. В качестве основных инфузионных сред используют кристаллоидные растворы, однако данные о влиянии сбалансированных многокомпонентных растворов на гемодинамический профиль у больных с тяжелой травмой в литературе практически отсутствуют.
Цель: исследовать возможности коррекции гемодинамических нарушений у больных с тяжелой сочетанной травмой с применением современного многокомпонентного препарата на основе 6%-го раствора сорбитола (реосорбилакта).
Материал и методы исследования: всего было обследовано 60 больных с тяжелой сочетанной травмой и клиникой травматического шока I–II степени в возрасте от 18 до 46 лет. Больные были разделены на две группы: 1-я группа (n = 30) — больные, которым в стандартный комплекс интенсивной терапии (ИТ) был включен реосорбилакт в дозе 8–10 мл/кг массы тела; 2-я группа (n = 30) — больные, которым проводился стандартный комплекс ИТ.
Результаты: введение реосорбилакта приводило к снижению объема внеклеточной жидкости, увеличению ОЦК и переходу гипокинетического режима кровообращения в эукинетический уже в течение первых часов после начала инфузии, который сохранялся до 6 часов после окончания инфузии (p < 0,01). Введения адреномиметиков требовали: перед началом исследования в 1-й и 2-й группах 7 (23,3 %) и 6 (20,0 %) больных, через 6 часов — соответственно 1 (3,3 %) и 4 (13,3 %), а через сутки после введения реосорбилакта ни один больной не нуждался во введении адреномиметиков, тогда как в группе 2 таких больных было 3 (10,0%, p < 0,05).
Выводы: Применение сбалансированных многокомпонентных растворов на основе сорбитола сопровождается изменением гипокинетического типа кровообращения на эукинетический, отсутствием гипергидратации интерстиция, быстрой стабилизацией показателей гемодинамики и уменьшением потребности в адреномиметической поддержке.
Конфликт интересов: отсутствует.
Ключевые слова: тяжелая травма, инфузионная терапия, реосорбилакт.
Выбор рациональной программы инфузионной терапии при тяжелой травме остается актуальной проблемой. Почти все шоковые состояния требуют большого объема инфузии в результате серьезного истощения внутрисосудистого объема. Первичная жидкостная ресусцитация пациентов после критических травм основывается на стратегии допустимой (управляемой) гипотензии, которая в англоязычной литературе описана словосочетанием «permissive hypotension» и является частью стратегии Damage Control (контроль повреждений) [1].
Основной целью инфузионной терапии должно быть не достижение показателей нормотензии, а ориентир на следующие критерии:
• сохранение сознания пациента;
• при проникающих ранениях (без сопутствующей тяжелой черепно-мозговой травмы) — поддержание систолического артериального давления на уровне 70–80 мм рт. ст., при тупой травме — 90 мм рт. ст.;
• при сопутствующей черепно-мозговой травме — поддержка среднего артериального давления, не менее 65 мм рт. ст. В случае сочетанной травмы прерогативой остается протекция головного мозга, так называемый подход ТТВ — Time To Brain («время для мозга»). В связи с этим большое значение приобретает адекватная, рационально выстроенная инфузионная терапия [2].
Инфузионная терапия при лечении пациентов с тяжелой травмой проводится с целью устранения гиповолемии, нарушений водно-электролитного и кислотноосновного балансов, реологических свойств крови, расстройств микроциркуляции и обмена веществ, для обеспечения эффективного транспорта кислорода и дезинтоксикации. Она оказывает многостороннее влияние на основные системы жизнеобеспечения организма. При этом выявляются волемический, реологический и гемодилюционный эффекты [3].
В качестве основных инфузионных сред используются кристаллоидные и коллоидные растворы. Изотонические электролитные растворы по составу близки к внеклеточной жидкости, однако имеют малый непосредственный волемический эффект (не более 20 % от объема введенной среды) [4]. Среди коллоидных растворов в последние годы все большую популярность приобретают растворы гидроксиэтилкрахмала в связи с их высоким волемическим эффектом и длительным периодом полувыведения при относительно небольшом количестве побочных реакций [4].
Какие же растворы рекомендуются для проведения коррекции гемодинамических нарушений в современных руководствах? Согласно Рекомендациям начальной ресусцитации пациентов с тяжелой сочетанной травмой (NICE guidelines, 2016. Major trauma: Assessment and Initial Management), считается, что кристаллоиды являются стартовыми инфузионными средствами для травмированных пациентов (класс 1B).
Применение гипертонических солевых растворов следует рассматривать у гемодинамически нестабильных пациентов (класс 2B). Использование коллоидов возможно в рекомендованных ограниченных дозах для гемодинамически нестабильных пациентов (степень 2С) [5]. Следует также помнить, что принципы Damage Control должны быть рутинно применены у тяжелых раненых пациентов с тяжелым геморрагическим шоком, признаками продолжающегося кровотечения и коагулопатии, гипотермии, ацидоза [5].
Одним из перспективных путей коррекции нарушений волемического состояния является «малообъемная» инфузия с применением гиперосмолярного полиэлектролитного сбалансированного раствора Реосорбилакт («Юрия-Фарм», Украина). Перспективность его применения в качестве препарата первой очереди при гиповолемическом шоке обусловлена в первую очередь гиперосмолярностью раствора. Высокую осмолярность раствора образуют осмотически активные вещества — сорбитол, натрия лактат и все имеющиеся ионы, в первую очередь ионы натрия. Осмолярность Реосорбилакта составляет 891 мосмоль/кг, что в 3 раза выше осмолярности плазмы.
Эффект гиперосмолярности реализуется следующим механизмами:
• повышение осмолярности плазмы и активация осморецепторов, активация симпатической нервной системы и увеличение продукции адренокортикотропного гормона и, как следствие, адреналина и норадреналина;
• снижение капиллярной утечки, соответственно, оттока жидкости в интерстиций;
• привлечение в сосудистое русло дополнительной жидкости из интерстициального и внутриклеточного пространства по осмотическому градиенту.
Большое значение в формировании высокой осмолярности реосорбилакта играют ионы натрия, концентрация которых в растворе превышает концентрацию в крови почти в 2 раза. По сути, Реосорбилакт содержит гипертонический солевой раствор. В то же время известно, что использование гипертонического раствора натрия хлорида приводит к увеличению ОЦК и уменьшению общего объема инфузии, улучшает функцию почек и уменьшает количество периоперационных осложнений и летальность у различных категорий пациентов [6, 7].
Благодаря высокой осмолярности Реосорбилакт вызывает поступление жидкости из межклеточного пространства в сосудистое русло, что способствует улучшению микроциркуляции и перфузии тканей [8].
Второе важное свойство — наличие натрия лактата, который является донатором резервной щелочности, имеет нейтральную реакцию, в сосудистом русле диссоциирует на ионы натрия и молочную кислоту, которая метаболизируется в печени до натрия бикарбоната, что повышает щелочность крови. Коррекция метаболического ацидоза при этом осуществляется медленно и без резких колебаний рН, в отличие от влияния натрия бикарбоната.
Заслуживает особого внимания то, что натрия лактат входит в «Ориентировочный перечень жизненно необходимых лекарственных средств», разработанный Всемирной организацией здравоохранения (ВОЗ) (англ. «WHO Model List of Essential Medicines»). Этот перечень ВОЗ состоит из наиболее эффективных и безопасных лекарственных средств, необходимых для удовлетворения самых важных потребностей в системе здравоохранения.
В последнем, 21-м издании (2019) натрия лактат входит в раздел 26 «Растворы, корректирующие водные, электролитные и кислотно-щелочные расстройства», подраздел 26.2 «Парентеральные растворы» [9]. Такое признание ВОЗ еще раз подтверждает эффективность и безопасность натрия лактата как компонента полифункциональных растворов.
Таким образом, перспективность использования реосорбилакта в инфузионной терапии волемических нарушений очевидна. В то же время данные о его влиянии на гемодинамический профиль у больных с тяжелой травмой в литературе практически отсутствуют. Это и обусловило цель проведенного исследования.
Цель
Авторы ставили перед собой цель исследовать возможности коррекции гемодинамических нарушений у больных с тяжелой сочетанной травмой с применением современного многокомпонентного препарата на основе 6%-го раствора сорбитола (реосорбилакта).
Материал и методы исследования
Нами были обследованы 60 больных в возрасте от 18 до 46 лет, находившихся на лечении в отделении интенсивной терапии общего профиля КНП КОС «Киевская областная клиническая больница». Больные были разделены на две группы: 1-я группа — пациенты с тяжелой сочетанной травмой и клиникой травматического шока I–II степени (n = 30), которым в стандартный комплекс интенсивной терапии (ИТ) был включен Реосорбилакт в дозе 8–10 мл/кг массы тела; 2-я группа — пациенты с сочетанной травмой и клиникой травматического шока I–II степени (n = 30), которым проводился стандартный комплекс ИТ. Указанные группы были репрезентативными по основным клиническим характеристикам (табл. 1).
Таблица 1. Общая характеристика пациентов в группах исследования, (M ± m)
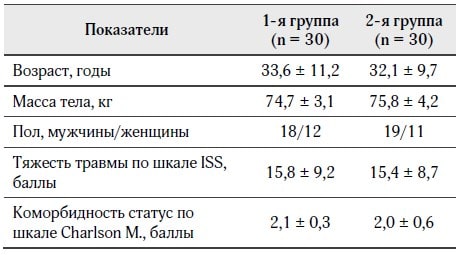
Средняя доза реосорбилакта у пациентов ОИТ составляла 8–10 мл/кг в сутки (600–800 мл/сут). С учетом того что реосорбилакт является гиперосмолярным раствором (около 900 мосмоль/л), его введение проводилось под контролем осмолярности крови и не назначалось больным с подтвержденным или подозреваемым гиперосмолярным состоянием.
Эффективность инфузионной терапии оценивали по общепринятым клиническим признакам, таким как: артериальное давление систолическое (СистАТ), диастолическое (ДАД) и среднее (САД), число сердечных сокращений (ЧСС) и SрO2 (%), которые определяли по показаниям монитора ЮМ-300 -10 («ЮТАС», Украина). После установки центрального венозного катетера измеряли уровень центрального венозного давления (ЦВД).
Динaмику ударного (УИ) и сердечного индекса (CИ), индекса мощности левого желудочка (ИМЛЖ), фракции выброса (ФВ), общего периферического сопротивления сосудов (ОПСС) изучали методом эхокардиографии, исследования с помощью аппарата SA 600 (Medison, Республика Корея). Объем внеклеточной жидкости (ОВЖ) определяли методом интегральной реографии тела по М. И. Тищенко с помощью компьютерного реоанализатора «Диамант-Р».
Исследования проводились на 5 этапах: перед началом, а также через 3, 6, 12 и 24 часа после введения препарата.
У всех пациентов обеих групп исследования применяли традиционный комплекс ИТ, который включал респираторную поддержку, аналгоседацию, ликвидацию нарушений водно-электролитного баланса и кислотнощелочного равновесия. В программу инфузионнотрансфузионной терапии по показаниям включали введение эритроцитарной массы и свежезамороженной плазмы. При необходимости проводили вазопрессорную и инотропную поддержку. Проводилась симптоматическая терапия.
Статистическую обработку результатов исследования проводили с использованием пакетов программ Excel-2010 и Statistica 6.0. Статистически значимой разницу между показателями считали при вероятности верности нулевой гипотезы менее 5 % (р < 0,05).
Результаты и их обсуждение
Перед началом инфузионной терапии у пациентов обеих групп наблюдались признаки умеренной гиповолемии (сниженные показатели САД, тахикардия, олигурия), а показатели инструментальных методов исследования демонстрировали гипокинетический тип центральной гемодинамики без достоверной разницы между группами больных (табл. 2).
Таблица 2. Показатели системной гемодинамики в исследуемых группах пациентов (M ± m)
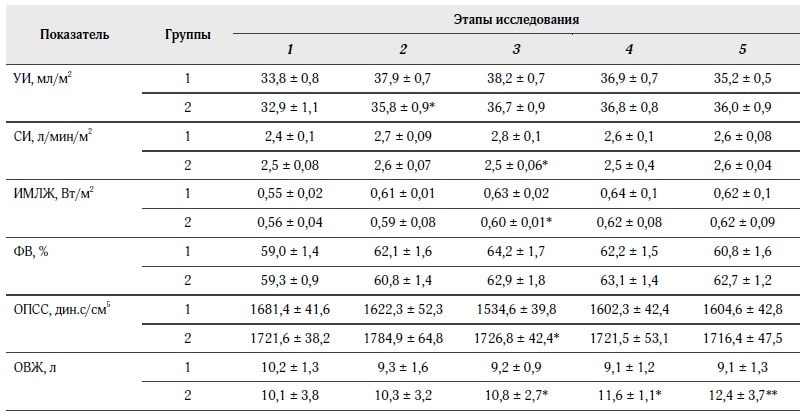 Примечания. * — разница между группами достоверна (p < 0,05); ** — разница между группами достоверна (p < 0,01).
Примечания. * — разница между группами достоверна (p < 0,05); ** — разница между группами достоверна (p < 0,01).
На втором этапе исследования (через 3 часа после начала инфузии) в первой группе больных наблюдали достоверное увеличение УИ, СИ и ФВ соответственно на 10,4, 12,5, 4,8 %, при этом ОВЖ снижался на 8,8 % (р < 0,05); ОПСС имел тенденцию к снижению — на 5,3 %. У больных второй группы на этом этапе достоверных изменений гемодинамических показателей не наблюдалось.
Через 6 часов после начала инфузии (III этап) в группе 1 сохранялась подобная гемодинамическая картина: УИ, СИ, ИМЛЖ и ФВ были достоверно выше исходных величин соответственно на 13,0, 16,6, 14,5 и 8,8 %, ОПСС и ОВЖ снижались соответственно на 9,2 и 9,8 % (р < 0,05). Через 12 часов (IV этап) после окончания инфузии отмечали дальнейшее увеличение показателя ИМЛЖ на 2,1 % по сравнению с предыдущим этапом, при этом ОВЖ был на 4,7 % ниже предыдущего этапа, а ОПСС выше соответственно на 14,7 % (р < 0,05). Во второй группе достоверных изменений на этих этапах не наблюдалось.
К концу суток (V этап) основные гемодинамические показатели в обеих группах больных приближались к референтным величинам, но в группе 1 показатели ОПСС и ОВЖ были ниже показателей в группе 2 соответственно на 6,7 и 26,6 % (р < 0, 01).
Таким образом, введение Реосорбилакта (8–10 мл/кг) приводило к достоверному снижению объема внеклеточной жидкости (через переход ее в внутрисосудистое русло), что совместно с объемом перелитого раствора приводило к увеличению ОЦК и переходу гипокинетического режима кровообращения в более благоприятный эукинетический.
Этот положительный гемодинамический эффект впервые появлялся уже в первые часы от начала инфузии и сохранялся до 6 часов после окончания инфузии. В дальнейшем наблюдали стабилизацию гемодинамических показателей в обеих группах, однако показатель объема интерстициальной жидкости, как и на предыдущих этапах, был достоверно ниже в группе 1 (p < 0,01).
Анализ клинических показателей гемодинамики также показал интересные результаты (табл. 3).
Таблица 3. Клинические показатели системной гемодинамики и потребность в адреномиметиках, (M ± m)
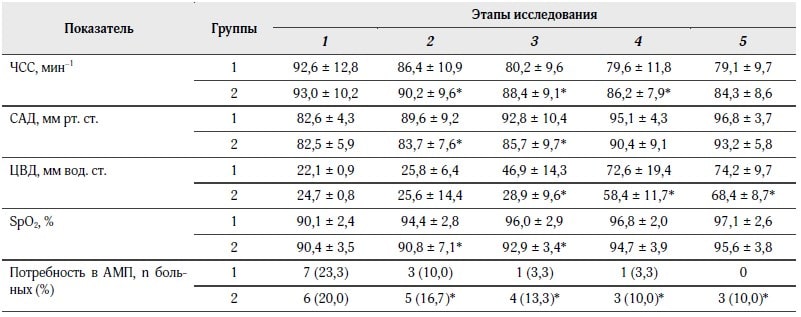 Примечания. * — разница между группами 1 и 2 достоверна (p < 0,05); АМП — адреномиметическая поддержка.
Примечания. * — разница между группами 1 и 2 достоверна (p < 0,05); АМП — адреномиметическая поддержка.
По ходу исследования в первой группе было выявлено снижение ЧСС на 6,7 % на втором этапе исследования и на 14,6 % — через 24 часа с момента инфузии реосорбилакта. Наоборот, показатели САД на 8,5 % были выше на втором этапе исследования, что указывало на эффективное восстановление дефицита ОЦК. Данная динамика также отображалась в увеличении показателя ЦВД, который у больных первой группы уже через 6 часов был выше на 112,2 % по сравнению с исходными значениями, тогда как в группе 2 на фоне инфузионной терапии произошло увеличение ЦВД только на 17,0 % (табл. 3).
Закономерным следствием улучшения гемодинамических показателей было и то, что больные в группе реосорбилакта меньше нуждались в адреномиметической поддержке. Так, если перед началом исследования в 1-й и 2-й группах было 7 (23,3 %) и 6 (20,0 %) таких больных, то уже через 6 часов — соответственно 1 (3,3 %) и 4 (13,3 %). А через сутки после введения реосорбилакта ни один больной не требовал введения адреномиметиков, тогда как в группе 2 таких больных было 3 (10,0 %, p < 0,05).
Следует отметить, что описанная программа ИТ в целом хорошо переносилась больными. В процессе лечения нами не было отмечено случаев возникновения побочных эффектов, характерных для использования кристаллоидов (отеки конечностей, острая сердечная недостаточность) или коллоидов (гипокоагуляция, нарушения функции почек), а уровни дефицита электролитов быстро (в течение 2–3 суток) возвращались к нормальным параметрам.
Выводы
- Лечение больных с тяжелой сочетанной травмой остается актуальной проблемой, для решения которой необходимо применять современную инфузионную терапию сбалансированными многокомпонентными растворами.
- Применение сбалансированных многокомпонентных растворов на основе сорбитола сопровождается изменением гипокинетического типа кровообращения на эукинетический, отсутствием гипергидратации интерстиция, быстрой стабилизацией показателей гемодинамики и уменьшением потребности в адреномиметической поддержке.
- Лечение с использованием растворов на основе сорбитола хорошо переносится и не сопровождается развитием осложнений, характерных для применения растворов коллоидов или классических кристаллоидов.
Авторы:
• Лоскутов Олег Анатольевич — д. м. н., профессор, заведующий кафедрой анестезиологии и интенсивной терапии НМАПО имени П. Л. Шупика
• Недашковский Сергей Михайлович — к. м. н., доцент кафедры анестезиологии и интенсивной терапии НМАПО имени П. Л. Шупика
• Бабак Сергей Иванович — заведующий отделением интенсивной терапии КНП КОС «Киевская областная клиническая больница»
• Дяченко Сергей Петрович — врач отделения интенсивной терапии КНП КОС «Киевская областная клиническая больница»
• Кедьо Борис Иванович — врач отделения интенсивной терапии КНП КОС «Киевская областная клиническая больница»
• Юркив Владимир Владимирович — врач отделения интенсивной терапии КНП КОС «Киевская областная клиническая больница»
• Галушко Александр Анатольевич — д. м. н., профессор, профессор кафедры анестезиологии и интенсивной терапии НМАПО имени П. Л. Шупика
Литература:
- Cannon JW, Khan MA, Raja AS, Cohen MJ, Como JJ, Cotton BA, et al. Damage control resuscitation in patients with severe traumatic hemorrhage. Journal of Trauma and Acute Care Surgery [Internet]. Ovid Technologies (Wolters Kluwer Health); 2017 Mar;82(3):605–17. Available from: https://doi.org/10.1097/ta.0000000000001333
- Babak SI, Kuchinskaya IA, Galushko OA, Dyachenko SP. Modern management strategies for infusion therapy for severe trauma. Emergency medicine. 2016;5(4):560–7.
- Shlapak IP, Golubovska OA, Halushko OA. [Dehydration syndrome]. Acute conditions and emergencies in medical practice. 2015;6:15–9. [In Ukrainian]
- Marino Paul L. Intensive care. Per. from English under the general. ed. A.P. Zilber. M.: GEOTAR-Media, 2010;768.
- Glen J, Constanti M, Brohi K. Assessment and initial management of major trauma: summary of NICE guidance. BMJ [Internet]. BMJ; 2016 Jun 22; i3051. Available from: https://doi.org/10.1136/bmj.i3051
- Orbegozo D, Vincent JL, Creteur J, Su F. Hypertonic Saline in Human Sepsis. Anesthesia & Analgesia [Internet]. Ovid Technologies (Wolters Kluwer Health); 2019 Jun;128(6):1175–84. Available from: https://doi.org/10.1213/ane.0000000000003955
- Pfortmueller CA, Schefold JC. Hypertonic saline in critical illness – A systematic review. Journal of Critical Care [Internet]. Elsevier BV; 2017 Dec;42:168–77. Available from: https://doi.org/10.1016/j.jcrc.2017.06.019
- Cherniy VI., Kolesnikov AN., Oleinikov KN., Egorov AA., Biloshapka VI. Rational infusion therapy. Donetsk: Publisher Zaslavsky A.Yu., 2012;184. [In Ukrainian]
- 21st World Health Organization Model List of Essential Medicines 2019. Access: https://apps.who.int/iris/bitstream/handle/10665/325771/WHOMVP-EMP-IAU-2019.06-eng.pdf?ua=1