Первые данные о результатах международного многоцентрового клинического исследование RheoSTAT-CP0691 по эффективности и безопасности инфузионного раствора Реосорбилакт® в комплексной терапии гнойного перитонита

Резюме: Генерализованные формы перитонита являются основным фактором смерти, не вызванной травмами, во всех случаях оказания неотложной помощи и второй ведущей причиной развития сепсиса у тяжелобольных пациентов. Целью данного исследования было оценить эффективность и безопасность многокомпонентного инфузионного раствора Реосорбилакт в терапии пациентов с диагнозом гнойного перитонита.
В международном многоцентровом рандомизированном исследовании принял участие 181 пациент в возрасте от 18 до 60 лет с диагнозом «гнойный перитонит». Пациенты получали терапию препаратом Реосорбилакт в дозировке согласно инструкции по применению препарата. Первичным показателем эффективности терапии рассматривалось изменение оценки по шкале SOFA на 3-й день терапии. В качестве вторичных показателей рассматривались изменения оценки по шкалам APACHE II, SAPS II, MODS и MPI, а также изменение маркеров эндогенной интоксикации на 3-й день терапии.
Безопасность препарата оценивалась с помощью анализа нежелательных явлений (НЯ) и жизненно важных показателей через 3 дня терапии. На 3-й день лечения Реосорбилактом были зафиксированы статистически значимые изменения оценки по шкалам SOFA (на 1,80±0,91 балла), MODS (на 1,45±0,76 балла) и MPI (на 1,84±5,03 балла). Кроме того, было выявлено статистически значимое улучшение маркеров эндогенной интоксикации (концентрации креатинина, билирубина, количество лейкоцитов, уровень С-реактивного белка, соотношение нейтрофилов и лимфоцитов) на 3-й день лечения. Большинство НЯ (98,99 %) были легкими.
Ни одно из НЯ не было связано с препаратом исследования и не привело к выбыванию пациента из исследования. Согласно полученным результатам RheoSTAT-CP0691, Реосорбилакт является эффективным и безопасным препаратом для лечения пациентов с гнойным перитонитом. Целесообразным является включение препарата Реосорбилакт в рутинные алгоритмы лечения пациентов с гнойным перитонитом.
Ключевые слова: абдоминальный сепсис, септический шок, перитонит, дезинтоксикационная терапия, инфузионная терапия, эффективность, безопасность, Реосорбилакт.
Введение
Острый генерализованный перитонит является угрожающей жизни интраабдоминальной патологией [1, 2]. Генерализованные формы перитонита выступают основным фактором, который приводит к смерти, не вызванной травмами, во всех случаях оказания неотложной помощи и второй ведущей причиной развития сепсиса у тяжелобольных пациентов [6, 7]. В случае непредоставления своевременной терапии у пациентов развиваются бактериемия, септицемия, септический шок и полиорганная дисфункция [4].
Терапия гнойного перитонита, которая может сопровождаться сепсисом и полиорганной недостаточностью, является одной из наиболее сложных и дискуссионных проблем в абдоминальной хирургии. За последние 10 лет частота гнойного перитонита стала увеличиваться, а надежда на решение проблемы только антибактериальными средствами не оправдалась. Летальность от распространенных форм перитонита, по данным различных исследований, составляет от 8 до 34 % [1, 3, 4, 7, 8].
Несмотря на значительный прогресс в эффективности лабораторных тестов, методов визуализации, периоперативной ресусцитации и хирургических техник, ведение пациентов с распространенными формами перитонита требует комплексного подхода и ставит сложные задачи перед хирургами и анестезиологами [4, 5, 9].
Успехи в лечении распространенного перитонита наряду с сохранением ведущей роли раннего хирургического вмешательства, своевременной ликвидацией источника перитонита, тщательной санацией и адекватным дренированием брюшной полости во многом зависят от подавления инфекции с помощью интенсивной антибактериальной терапии, борьбы с интоксикацией, устранения пареза кишечника, предотвращения вторичных осложнений и рациональной до- и послеоперационной интенсивной терапии, направленной на устранение гемодинамических нарушений, коррекцию объемных и метаболических сдвигов, а также от восстановления и поддержания на оптимальном уровне функций жизненно важных органов и систем.
Современная антибактериальная терапия, методы интра- и экстракорпоральной детоксикации, несомненно, позволили добиться определенных положительных результатов в лечении перитонита, но конечные результаты его до сих пор нельзя считать удовлетворительными. Поэтому необходимы исследования и разработки новых терапевтических алгоритмов детоксикации и улучшения реологических показателей крови у пациентов с перитонитом.
В соответствии с рекомендациями по ведению абдоминального сепсиса Американской ассоциации инфекционных заболеваний, у пациентов с перитонитом следует проводить быструю инфузионную терапию с целью восстановления объема циркулирующей крови (ОЦК). В случае развития септического шока ресусцитацию следует начинать немедленно после выявления гипотензии. У пациентов без признаков снижения ОЦК внутривенная инфузионная терапия должна проводиться при подозрении на интраабдоминальную инфекцию [10].
В консенсусе Всемирного общества по неотложной хирургии, посвященном ведению интраабдоминальных инфекций, отмечается, что проведение инфузионной терапии для улучшения микрососудистого кровотока и увеличения минутного объема крови является неотъемлемой составляющей терапии абдоминального сепсиса. Основная цель проведения инфузионной терапии — повышение системного артериального давления (АД). Согласно консенсусу, препаратами первой линии являются кристаллоидные инфузионные растворы, характеризующиеся высоким профилем переносимости и экономически доступные [11].
После стабилизации гемодинамических показателей (достижение уровня среднего АД в пределах от 65 до 90 мм рт. ст.) у пациентов с генерализованным перитонитом рекомендуется применять рестриктивный тип инфузионной терапии, то есть исключить возможность введения чрезмерного объема инфузии, что может усилить отек в брюшной полости, повысить интраабдоминальное давление, а также вызвать другие неблагоприятные воздействия — от повреждения гликокаликса до снижения функции почек [11-17].
Поскольку решить все задачи инфузионной терапии и одновременно избежать нежелательной перегруженности жидкостью с помощью монокомпонентных растворов крайне сложно, все шире применяются поликомпонентные инфузионные препараты. Чтобы оценить эффективность поликомпонентной инфузионной терапии в комплексном лечении перитонита, было проведено международное многоцентровое клиническое исследование RheoSTAT-CP0691.
Объектом исследования выступил препарат полифункционального действия Реосорбилакт®, в состав которого входят: сорбитол — 60 г, натрия лактат — 19 г, натрия хлорид — 6 г, кальция хлорид — 0,1 г, калия хлорид — 0,3 г, магния хлорид — 0,2 г, вода для инъекций — до 1 л. Осмолярность препарата — 891 мОсм/л, рН — 6,0–7,6. Задача данного исследования — оценить следующие показатели у пациентов с гнойным перитонитом, получавших терапию препаратом Реосорбилакт:
- динамикубалловпо интегральным шкалам SOFA (Sepsis-related Organ Failure Assessment), MODS (Multiple Organ Dysfunction) и MPI (Mannheim Peritonitis Index);
- динамику биохимических показателей эндогенной интоксикации;
- динамику иммунологических показателей эндогенной интоксикации;
- динамику интегральных показателей эндогенной интоксикации;
- безопасность исследуемого препарата по частоте нежелательных явлений (НЯ) и общей выживаемости.
Материалы и методы
Был проведен электронный поиск в англоязычных источниках базы данных PubMed за последние 20 лет по ключевым словам «peritonitis», «purulent peritonitis», «septic shock», «fluid resuscitation», «sepsis resuscitation», «infusion». Также был проанализирован обзор результатов международного многоцентрового открытого РКИ IV фазы с ослепленной оценкой конечных точек эффективности RheoSTAT-CP0691 на основании отчета, предоставленного компанией «Юрия-Фарм».
РКИ RheoSTAT включало 629 пациентов с сепсисом, перитонитом, ожоговой болезнью и пневмонией, которые лечились в 37 клинических центрах 6 стран. В субисследовании RheoSTAT-CP0691 peritonitis принимали участие 181 пациент из 10 клинических центров 4 стран – Украины, Молдовы, Грузии и Узбекистана согласно принципам, изложенным в Хельсинской декларации Всемирной медицинской ассоциации, а также принципам качественной клинической практики (ICH E6 GCP) и национальных стандартов стран-участниц.
Процедура получения информированного согласия пациента соответствовала национальным стандартам стран-участниц, требованиям надлежащей клинической практики ICH E6 GCP и этическим принципам, изложенным в текущей версии Хельсинкской декларации. Дизайн исследования представлен на рис. 1.
Критерии включения пациентов в субисследование RheoSTAT-CP0691:
- мужчины и женщины в возрасте от 18 до 60 лет включительно;
- 24 часа и меньше с момента установления при первичной лапаротомии и ревизии брюшной полости диагноза «гнойный перитонит» (распространенный или тотальный, то есть в двух и более анатомических отделах брюшной полости) с индексом MPI от 21 до 29 баллов, что соответствует 2-й степени тяжести и реактивной фазе согласно унифицированному клиническому протоколу оказания медицинской помощи больным с острым перитонитом;
- собственноручно подписанное пациентом информированное согласие на участие;
- начальное значение по шкале SOFA 2 балла и выше.
В качестве исследуемого препарата применялся Реосорбилакт®, раствор для инфузий, который вводился внутривенно капельно в дозах (объемах) в соответствии с инструкцией по применению в течение 3 дней.
Анализ данных осуществлялся в следующих популяциях:
- популяция всех включенных пациентов (intent-to-treat, ITT): все рандомизированные пациенты, которым была назначена и введена хотя бы одна инфузия исследуемого препарата и у которых есть данные о балах SOFA как до, так и после применения исследуемого препарата или препарата сравнения;
- популяция по протоколу (perprotocol, PP): все рандомизированные пациенты, которые завершили участие в исследовании в соответствии с протоколом (закончили предложенный период лечения и наблюдения без существенных отклонений);
- популяция безопасности (safety): все рандомизированные пациенты, которые применили хотя бы одну дозу исследуемого препарата или препарата сравнения и завершили хотя бы один визит оценки параметров безопасности.
Оценка безопасности проводилась на протяжении всего исследования. НЯ считалось любое обнаруженное у субъекта клинического исследования после применения лекарственного препарата неблагоприятное с медицинской точки зрения событие, которое может и не иметь причинно-следственной связи с его применением.
То есть НЯ могло представлять собой любой неблагоприятный симптом (включая отклонение лабораторного показателя от нормы), жалобу или заболевание, время возникновения которого не исключает причинно-следственной связи с применением лекарственного (исследуемого) продукта вне зависимости от наличия или отсутствия такой связи. Как серьезное НЯ (СНЯ) рассматривалось любое неблагоприятное с медицинской точки зрения событие, которое:
- привело к смерти;
- было угрожающим жизни;
- стала причиной постоянной/устойчивой инвалидности или нетрудоспособности;
- потребовало госпитализации в стационар или стало причиной продления сроков текущей госпитализации;
- обусловило врожденную аномалию / дефект развития.
Кроме того, в качестве СНЯ фиксировалось любое событие, которое формально не подходило к вышеперечисленным критериям, но было значимым, с точки зрения исследователя, медицинским событием. Все остальные НЯ, не соответствующие этим критериям, расценивались как «несерьезные».
В исследование был включен всего 181 пациент, из этого количества 90 были рандомизированы в группу препарата Реосорбилакт. В популяцию ITT были включены 74/90 (82,22 %) пациентов из группы Реосорбилакта. В популяцию по протоколу вошли 73/90 (81,11 %) пациентов. В популяцию безопасности вошли все рандомизированные пациенты.
Основным параметром эффективности в этом исследовании было изменение общего балла по шкале SOFA на 3-й день по сравнению с исходным значением при поступлении, рассчитанное как разница средних (значение показателя на момент включения в исследование за вычетом значения показателя в конце лечения).
Дополнительно, в качестве вторичных параметров эффективности, оценивался широкий спектр биохимических маркеров, иммунологических критериев и интегральных показателей тяжести эндогенной интоксикации, характерной для пациентов с распространенным гнойным перитонитом. Критерии оценки эффективности и безопасности представлены в табл. 1.
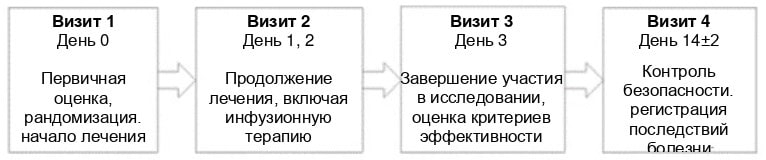 Рис. 1. Схема дизайна исследования RheoSTAT-CP0691
Рис. 1. Схема дизайна исследования RheoSTAT-CP0691
Визит 1 День 0
Первичная оценка, рандомизация, начало лечения
Визит 2 Дни 1, 2
Продолжение лечения, включая инфузионную терапию
Визит 3 День 3
Завершение участия в исследовании, оценка критериев эффективности
Визит 4 День 14 ± 2
Контроль безопасности, регистрация последствий болезни
Табл. 1. Критерии оценки эффективности и безопасности в исследовании RheoSTAT-CP0691
|
Оценка эффективности проводилась путем сравнения исходных показателей при госпитализации и показателей на 3-й день терапии |
|
Основной параметр: изменение общего балла по шкале SOFA Вторичные параметры: • Изменение общего балла по шкалам APACHE II, SAPS II, MODS и MPI • Оценка эндогенной интоксикации на основании: – биохимических маркеров: концентрации в сыворотке крови глюкозы, натрия, калия, мочевины, креатинина, общего билирубина, аланинаминотрансферазы (АлАТ), аспартатаминотрансферазы (АсАТ), γ-глутамилтрансферазы, щелочной фосфатазы, лактатдегидрогеназы, креатинфосфокиназы, прокальцитонина, альбуминовой фракции, стандартного бикарбоната и лактата; – иммунологических критериев: количественное содержание лейкоцитов, лимфоцитов, тромбоцитов с расчетом лейкоцитарного, ядерного и гематологического индексов интоксикации (II), отношение нейтрофилов и лимфоцитов, концентрация С-реактивного белка (СРБ), иммуноглобулинов, интерлейкинов 1 и 2, компонентов комплемента 3 и 4 ; – клинических признаков (адинамия, апатия, слабость, нарушение памяти, сна, раздражительность, анорексия), параметров электрокардиограммы, показателей центральной гемодинамики и оценки сознания по шкале Глазго |
|
Оценка безопасности |
|
• Общая частота НЯ • Частота СНЯ • Частота НЯ, связанных с применением исследуемого препарата • Частота НЯ, которые привели к выбыванию пациента из исследования • Частота НЯ, ранее описанных в инструкции по использованию исследуемого препарата • Частота возникновения полиорганной недостаточности • Общая выживаемость пациентов (%) в ходе дальнейшего наблюдения (день 14 ± 2) |
Результаты и их обсуждение
Существуют два основных класса инфузионных средств — коллоиды и кристаллоиды. К коллоидам относят альбумин, гидроксиэтилкрахмал и желатин. Благодаря онкотической активности коллоиды теоретически должны были бы замедлять капиллярную утечку. Однако у пациентов с тяжелой инфекцией этот эффект довольно кратковременный из-за повреждения гликокаликса [18, 19]. По сравнению с кристаллоидами, коллоиды имеют несколько более длительный период полувыведения из внутрисосудистого пространства, хотя капиллярная утечка влияет на оба класса [20].
Другие гипотетические преимущества коллоидов включают противовоспалительный эффект и способность к поглощению оксида азота, но это касается только альбумина [21]. На сегодняшний день нет ни одного большого рандомизированного контролируемого исследования РКИ, которое доказывало бы четкую разницу в смертности между инфузионной терапией с помощью кристаллоидов или коллоидов в случае пневмонии или сепсиса.
Достаточно большим было РКИ SAFE с участием критически больных взрослых, в котором сравнивали 0,9%-й раствор хлорида натрия и альбумин как средства жидкостной ресусцитации. Несмотря на отсутствие значимой разницы в 28-дневной смертности в общей группе, указывали на лучшие результаты при использовании альбумина у пациентов с тяжелым сепсисом и острым респираторным дистресс-синдромом, но худшие — у пациентов с тяжелым травматическим поражением мозга [22, 23].
Растворы гидроксиэтилкрахмала связывают с острым повреждением почек у критически больных лиц, в связи с чем данные растворы признаны опасными в США и Европе [24, 25]. Последние международные руководства по ведению сепсиса не рекомендуют использовать коллоиды как начальный раствор для жидкостной ресусцитации из-за отсутствия преимуществ и чрезмерных расходов [26].
Среди кристаллоидов можно выделить небуферные растворы (изотонический раствор натрия хлорида) и буферные мультиэлектролитные растворы, которые отличаются по своему составу, концентрации хлоридов, рН и осмолярности, но более приближены к плазме, чем изотонический раствор натрия хлорида. Ресусцитация с применением 0,9%-го раствора натрия хлорида связана с возникновением гиперхлоремического метаболического ацидоза, острого повреждения почек и опасных функциональных нарушений со стороны жизненно важных органов [27-30].
Несмотря на это, изотонический раствор натрия хлорида сегодня остается самым употребляемым кристаллоидным раствором [31], который также часто используют как растворитель для введения различных лекарственных средств [28]. Два недавних РКИ SALT-ED и SMART указывают на явные преимущества сбалансированных буферных растворов перед изотоническим раствором натрия хлорида.
Хотя разницы в краткосрочной смертности не было, введение 0,9%-го раствора натрия хлорида ассоциировалось с высоким риском острого повреждения почек, включая смерть, потребность в диализе или длительное нарушение функции почек [29, 30].
Особого внимания заслуживают инфузионные растворы, содержащие многоатомные спирты, прежде всего сорбитол, который имеет ряд преимуществ:
- Благодаря более медленному превращению в моносахариды утилизируется лучше, чем глюкоза, и не вызывает углеводной перегрузки;
- После введения быстро включается в общий метаболизм (80 % утилизируется печенью, 5 % откладывается в тканях мозга, миокарде и скелетных мышцах, остальная часть выделяется с мочой или используется для неотложных энергетических потребностей);
- Устраняет обусловленный ацетилхолином спазм кишечника, стимулирует перистальтику без резкого ее усиления, что обосновывает его использование в послеоперационный период;
- В гипертонической концентрации оказывает значительную противоотечное действие, в частности способствует обратному развитию отека легких, характеризуется осмотическим диуретическим эффектом, что важно в условиях олигоанурии и острого повреждения почек;
- Благодаря мощному холецистокинетическому и холеретическому действию способствует восстановлению нормальной функции пищеварительной системы, имеет доказанный терапевтический эффект при острых и хронических гепатитах и токсических поражениях печени;
- В изотонической концентрации действует как дезагрегант, улучшая микроциркуляцию и перфузию тканей.
Среди сорбитолосодержащих средств следует отметить комплексный инфузионный препарат полифункционального действия Реосорбилакт® производства компании «Юрия-Фарм» (Украина). Кроме сорбитола, он содержит другие важные электролиты — калий, кальций и магний, но содержание хлоридов в нем лишь 112,7 ммоль/л, что уменьшает риск гиперхлоремического ацидоза.
Другим важным компонентом Реосорбилакта является натрия лактат, который обеспечивает щелочное воздействие, повышает резервную и титруемую щелочность крови, корректирует метаболический ацидоз, часто усложняющий тяжелые инфекции, сепсис, перитонит, кишечную непроходимость, почечную недостаточность, ожоги, шок, хроническую гипоксию и т. п.
Положительно влияет на работу сердца, регенерацию и дыхательную функцию крови, стимулирует функции системы мононуклеарных фагоцитов, оказывает дезинтоксикационное действие, усиливает диурез, улучшает работу почек и печени. Концентрация натрия лактата в Реосорбилакте в 5–6 раз выше (160–180 ммоль/л), чем в большинстве инфузионных растворов, что обеспечивает мощный лечебный эффект.
Наличие в составе Реосорбилакта двух компонентов с синергическим дезинтоксикационным действием и способностью коррекции кислотно-щелочного и водно-электролитного баланса ставит этот препарат в один ряд с мощнейшими дезинтоксикационными средствами [32]. Успешный опыт применения Реосорбилакта для дезинтоксикации и нормализации реологии крови у пациентов с такими тяжелыми гнойно-воспалительными заболеваниями, как перитонит [33], деструктивный панкреатит [34], синдром диабетической стопы [35], позволяет предполагать улучшение клинических последствий при пневмонии.
В дополнение в одном из клинических исследований установлено, что введение Реосорбилакта больным пневмонией способствует ранней нормализации температуры тела, исчезновению проявлений астеновегетативного синдрома и сокращению средней продолжительности госпитализации, стабилизации кислотно-основного состояния и показателей коагулограммы [36].
Изменение общего балла по шкале SOFA на 3-й день по сравнению с исходным значением при поступлении
Популяция ITT
При поступлении среднее значение (± стандартное отклонение) по шкале SOFA составляло 2,38 ± 0,59 балла в группе Реосорбилакта. На 3-й день среднее значение по шкале SOFA было равно 0,58 ± 0,84 балла. Среднее изменение оценки по шкале SOFA на 3-й день по сравнению с исходным уровнем составило 1,80 ± 0,91 балла.
В ходе дополнительного анализа было выявлено, что изменения среднего значения по шкале SOFA на 3-й день по сравнению со значениями при поступлении были статистически значимыми (р <0,001) у пациентов, получавших Реосорбилакт (рис. 1).
Популяция PP
При поступлении среднее значение (± стандартное отклонение) по шкале SOFA составляло 2,37 ± 0,59 балла. На 3-й день терапии Реосорбилактом среднее значение по шкале SOFA было равно 0,55 ± 0,80 балла. Среднее изменение оценки по шкале SOFA на 3-й день по сравнению с исходным уровнем составило 1,82 ± 0,89 (рис. 2).
Изменение общего балла по шкале MODS на 3-й день по сравнению с исходным значением при поступлении
Популяция ITT
При поступлении среднее значение (± стандартное отклонение) по шкале MODS составляло 2,22 ± 1,11 балла. На 3-й день среднее значение по шкале MODS было равно 0,77 ± 1,27 балла в группе Реосорбилакта. Среднее изменение оценки по шкале MODS на 3-й день по сравнению с исходным уровнем составило 1,45 ± 0,76 балла.
В ходе дополнительного анализа выявлено, что изменения среднего значения по шкале MODS на 3-й день по сравнению со значениями при поступлении в группе Реосорбилакта были статистически значимыми (р <0,001) (рис. 1).
Популяция РР
При поступлении среднее значение (± стандартное отклонение) по шкале MODS составляло 2,21 ± 1,12 балла в группе Реосорбилакта. На 3-й день среднее значение по шкале MODS было равно 0,75 ± 1,27 балла. Среднее изменение оценки по шкале MODS на 3-й день по сравнению с исходным уровнем составило 1,45 ± 0,76 балла (рис. 2).
Изменение общего балла по шкале MPI на 3-й день по сравнению с исходным значением при поступлении
Популяция ITT
При поступлении среднее значение (± стандартное отклонение) по шкале MPI составляло 22,61 ± 2,27 балла. На 3-й день среднее значение по шкале MPI у пациентов, получавших Реосорбилакт, было равно 20,77 ± 5,43 балла. Среднее изменение оценки по шкале MPI на 3-й день по сравнению с исходным уровнем составило 1,84 ± 5,03 балла.
В ходе дополнительного анализа было выявлено, что изменения среднего значения по шкале MPI на 3-й день по сравнению со значениями при поступлении были статистически значимыми (рис. 2).
Популяция PP
При поступлении среднее значение (± стандартное отклонение) по шкале MPI составляло 22,62 ± 2,28 балла. На 3-й день среднее значение по шкале MPI у пациентов, получавших Реосорбилакт, было равно 20,92 ± 5,31 балла. Среднее изменение оценки по шкале MPI на 3-й день по сравнению с исходным уровнем составило 1,70 ± 4,92 балла (рис. 3).
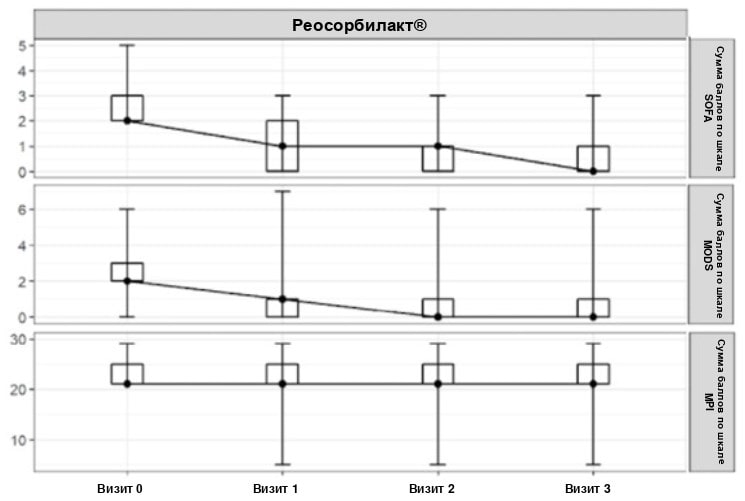 Рис. 2. Оценка по шкалам SOFA, MODS и MPI в ITT-популяции
Рис. 2. Оценка по шкалам SOFA, MODS и MPI в ITT-популяции
Визит 0 Визит 1 Визит 2 Визит 3
Сумма баллов по шкале SOFA Сумма баллов по шкале MODS
Сумма баллов по шкале MPI Реосорбилакт
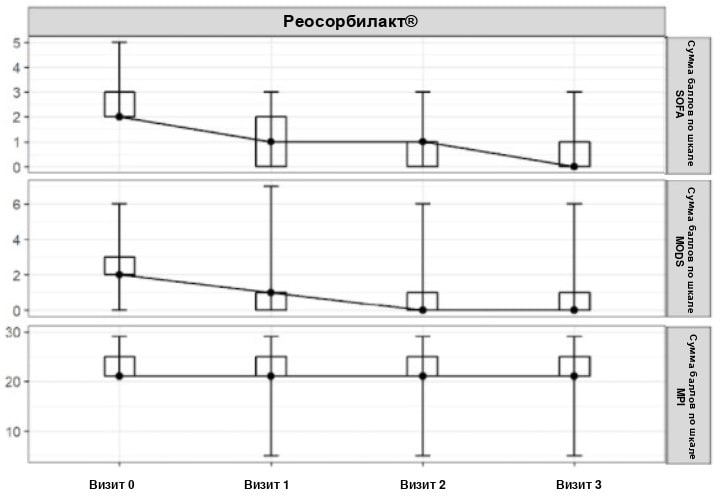 Рис. 3. Оценка по шкалам SOFA, MODS и MPI в PP-популяции
Рис. 3. Оценка по шкалам SOFA, MODS и MPI в PP-популяции
Визит 0 Визит 1 Визит 2 Визит 3
Сумма баллов по шкале SOFA Сумма баллов по шкале MODS
Сумма баллов по шкале MPI Реосорбилакт
Изменения маркеров эндогенной интоксикации в ITT-популяции (уровни лейкоцитов, лимфоцитов, СРБ, билирубина и креатинина)
При поступлении медиана (межквартильный диапазон) числа лейкоцитов составляла 10,95 (9,62–11,95) × 109/л в группе Реосорбилакта. На 3-й день медиана (межквартильный диапазон) числа лейкоцитов была равна 7,10 (6,00–8,43) × 109/л в группе Реосорбилакта. При дополнительном анализе выявлено, что изменения числа лейкоцитов на 3-й день по сравнению со значениями при поступлении были статистически значимыми (р <0,001).
При поступлении медиана (межквартильный диапазон) концентрации СРБ составляла 10,00 (6,00–14,00) мг/л в группе Реосорбилакта. На 3-й день медиана (межквартильный диапазон) концентрации СРБ была равна 0,00 (0,00–21,00) мг/л в группе Реосорбилакта. При дополнительном анализе выявлено, что изменения среднего значения концентрации СРБ на 3-й день по сравнению со значениями при поступлении были статистически значимыми (р <0,001).
При поступлении медиана (межквартильный диапазон) соотношения нейтрофилов и лимфоцитов составляла (4,00–7,61) в группе Реосорбилакта. На 3-й день медиана (межквартильный диапазон) соотношение нейтрофилов и лимфоцитов была равна 4,08 (3,64–4,59) в группе Реосорбилакта. При дополнительном анализе выявлено, что изменения среднего значения соотношения нейтрофилов и лимфоцитов на 3-й день по сравнению со значениями при поступлении внутри групп были статистически значимыми (р <0,001).
При поступлении медиана (межквартильный диапазон) концентрации общего билирубина составила 16,00 (12,00–17,90) мкмоль/л в группе Реосорбилакта. На 3-й день медиана (межквартильный диапазон) концентрации общего билирубина была равна 11,15 (7,00–15,82) мкмоль/л в группе Реосорбилакта. При дополнительном анализе выявлено, что изменения среднего значения концентрации общего билирубина на 3-й день по сравнению со значениями при поступлении были статистически значимыми (р <0,001).
При поступлении медиана (межквартильный диапазон) концентрации креатинина составляла 102,00 (84,50–109,00) ммоль/л в группе Реосорбилакта. На 3-й день медиана (межквартильный диапазон) концентрации креатинина была равна 90,00 (70,00–102,00) ммоль/л в группе Реосорбилакта. При дополнительном анализе выявлено, что изменения среднего значения концентрации креатинина на 3-й день по сравнению со значениями при поступлении были статистически значимыми (основная группа: р <0,001).
Динамика показателей биохимического анализа крови в PP-популяции на 3-й день терапии продемонстрирована на рис. 4.
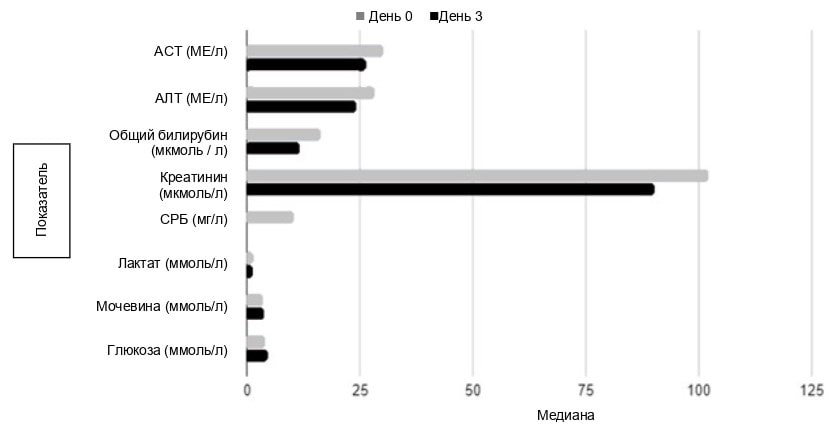 Рис. 4. Изменение медианы показателей биохимического анализа крови на 3-й день терапии Реосорбилакт в PP-популяции
Рис. 4. Изменение медианы показателей биохимического анализа крови на 3-й день терапии Реосорбилакт в PP-популяции
Показатель Медиана
День 0 День 3
АсАТ, МЕ/л АлАТ, МЕ/л
Общий билирубин, мкмоль/л
Креатинин, мкмоль/л
СРБ, мг/л Лактат, ммоль/л
Мочевина, ммоль/л Глюкоза, ммоль/л
Анализ нежелательных явлений
За время исследования НЯ были зарегистрированы у 63 пациентов (890 НЯ) группы Реосорбилакта. Всего было зарегистрировано 1 НЯ, расцененное как связанное с исследуемым препаратом, у 1 пациента в основной группе. Всего в исследовании были зарегистрированы 3 СНЯ (2 СНЯ в группе Реосорбилакта). Ни одно из СНЯ не было связано с исследуемым препаратом и не привело к выбыванию пациента из исследования. Согласно результатам анализа безопасности, применение препарата Реосорбилакт имеет приемлемый профиль безопасности.
Из 890 НЯ, зарегистрированных в группе Реосорбилакта, 881 НЯ (98,99 %) было легкой степени тяжести, 6 НЯ (0,67 %) — средней степени тяжести и 3 тяжелых НЯ (0,34 %). Не были зарегистрированы СНЯ, которые привели бы к выбыванию пациентов из исследования. Также не были зарегистрированы СНЯ, связанные с исследуемым препаратом; скорее всего, они были связаны с основным заболеванием (гнойным перитонитом). Общая выживаемость в группе Реосорбилакта на 14-й день с начала исследования составила 100 %.
Жизненно важные показатели
При поступлении медиана (межквартильный диапазон) температуры тела составляла 37,00 °С. На 3-й день терапии медиана (межквартильный диапазон) температуры тела была равна 36,60 (36,60–36,80) °С.
При поступлении медиана (межквартильный диапазон) частоты сердечных сокращений (ЧСС) составляла 88,00 (82,50–90,00) уд/мин. На 3-й день терапии Реосорбилактом медиана (межквартильный диапазон) ЧСС снизилась до 82,00 (76,00–86,00) уд/мин.
При поступлении медиана (межквартильный диапазон) систолического артериального давления (САД) составляла 115,00 (110,00–120,00) мм рт. ст. На 3-й день терапии медиана (межквартильный диапазон) САД была равна 120,00 (115,00–120,00) мм рт. ст.
При поступлении медиана (межквартильный диапазон) диастолического артериального давления (ДАД) составляла 75,00 (70,00–80,00) мм рт. ст. На 3-й день терапии Реосорбилактом медиана (межквартильный диапазон) ДАД была равна 75,00 (70,00–80,00) мм рт. ст.
При поступлении медиана (межквартильный диапазон) частоты дыхания (ЧД) составляла 18,00/мин (17,00–18,00). На 3-й день терапии медиана (межквартильный диапазон) ЧД былп равна 18,00/мин (17,00–18,00).
Результаты электрокардиографии
При поступлении средняя (± стандартное отклонение) ЧСС составила 88,00 ± 11,40 уд/мин. На 3-й день терапии средняя (± стандартное отклонение) ЧСС равна 82,12 ± 11,67 уд/мин.
При поступлении медиана (межквартильный диапазон) продолжительности интервала PR составляла 106,00 (102,00–141,50) мс. На 3-й день медиана (межквартильный диапазон) продолжительности интервала PR была равна 126,00 (104,00–146,00) мс.
При поступлении медиана (межквартильный диапазон) ширины комплекса QRS составляла 0,10 (0,09–0,10) с. На 3-й день медиана (межквартильный диапазон) ширины комплекса QRS была равна 0,10 (0,09–0,10) с.
При поступлении медиана (межквартильный диапазон) продолжительности интервала QT составляла 0,35 (0,33–0,37) с. На 3-й день медиана (межквартильный диапазон) продолжительности интервала QT была равна 0,36 (0,34–0,38) с.
При поступлении медиана (межквартильный диапазон) продолжительности интервала QTс составляла 0,39 (0,37–0,42) с. На 3-й день медиана (межквартильный диапазон) продолжительности интервала QTс была равна 0,40 (0,38–0,42) с.
При поступлении у 5,68% (n = 5/90) пациентов были выявлено клинически значимые отклонения результатов электрокардиографии. На 3-й день у 2,27% (n = 2/90) пациентов были выявлено клинически значимые отклонения.
Уже на 3-й день терапии у большинства пациентов наблюдались нормализация температуры тела, функции почек и улучшение оценки по большинству шкал оценки, используемых в исследовании (табл. 2).
Табл. 2. Параметры оценки эффективности препарата Реосорбилакт до и после терапии*
|
Показатели, единицы |
Начальные |
На 3-й день |
Р |
||||
|
n |
Ме |
МКД |
n |
Ме |
МКД |
||
|
Сумма баллов по шкале |
|||||||
|
SOFA |
74 |
2 |
2–3 |
74 |
0 |
0–1 |
<0,001 |
|
APACHE II |
74 |
3 |
2–5 |
74 |
3 |
1–4 |
0,118 |
|
SAPS II |
74 |
14 |
8–18 |
74 |
14 |
8–16 |
0,121 |
|
MODS |
74 |
2 |
2–3 |
74 |
0 |
0–1 |
<0,001 |
|
MPI |
74 |
21 |
21–25 |
74 |
21 |
21–25 |
0,005 |
|
Температура тела, °С |
74 |
37 |
36,80–37,40 |
74 |
36,6 |
36,6–36,8 |
<0,001 |
|
ЧСС, уд/мин |
74 |
88,5 |
84,25–90,00 |
74 |
82 |
78,25–88,00 |
<0,001 |
|
САД, мм рт. ст. |
74 |
115 |
110–120 |
74 |
115 |
110–125 |
0,331 |
|
ДАД, мм рт. ст. |
74 |
75 |
70–80 |
74 |
75 |
70–80 |
0,071 |
|
ЧД за 1 мин |
74 |
18 |
17–18 |
74 |
17 |
17–18 |
0,006 |
|
Мочевина, ммоль/л |
74 |
3,4 |
3,00–4,50 |
74 |
3,60 |
3,00–4,58 |
0,477 |
|
Креатинин, мкмоль/л |
74 |
102,00 |
84,50–109,00 |
74 |
90,00 |
80,00–102,00 |
<0,001 |
|
Общий билирубин, мкмоль/л |
74 |
16,00 |
12,00–17,90 |
74 |
11,15 |
7,00–15,82 |
<0,001 |
|
АлАТ, МЕ/л |
74 |
28,00 |
22,00–30,00 |
74 |
24,00 |
20,00–30,00 |
0,022 |
|
АсАТ, МЕ/л |
74 |
30,00 |
24,00–32,75 |
74 |
26,00 |
22,00–32,00 |
0,015 |
|
Альбуминовая фракция, % |
15 |
63,80 |
58,00–65,25 |
15 |
61,50 |
57,22–63,87 |
0,397 |
|
CРБ, мг/л |
73 |
10,00 |
6,00–14,00 |
73 |
0,00 |
0,00–10,00 |
<0,001 |
|
Тромбоциты, ×109/л |
74 |
210,00 |
190,00-235,25 |
74 |
220,00 |
194,00–301,25 |
<0,001 |
|
Лейкоциты, ×109/л |
74 |
10,95 |
9,62–11,95 |
74 |
7,10 |
6,00–8,43 |
<0,001 |
|
Ядерный ІІ |
62 |
0,05 |
0,05–0,09 |
63 |
0,05 |
0,03–0,06 |
<0,001 |
|
Лейкоцитарный ІІ |
62 |
4,20 |
2,37–4,31 |
63 |
1,64 |
0,79–4,10 |
<0,001 |
|
Гематологический ІІ |
62 |
4,00 |
3,82–4,32 |
63 |
3,35 |
2,57–4,00 |
<0,001 |
|
Индекс нейтрофилы/лимфоциты |
62 |
4,44 |
4,00–7,61 |
64 |
4,08 |
3,64–4,59 |
<0,001 |
Примечания: * данные из отчета о результатах РКИ RheoSTAT-CP0691, предоставленного компанией «Юрия-Фарм»; n — количество наблюдений; Ме (МКД) — медиана (межквартильный диапазон).
Обсуждение
С учетом того что пациенты с гнойным перитонитом 2-й степени тяжести оцениваются как имеющие сепсис, первичным критерием эффективности терапии была выбрана шкала SOFA, которая позволяет определять в количественном выражении тяжесть органно-системных нарушений и контролировать эффективность терапии в динамике у больных с сепсисом.
В связи с тем, что популяция пациентов с гнойным перитонитом и сепсисом является гетерогенной не только по характеру и выраженности органной недостаточности, но и по возрасту и коморбидным состояниям, что отражается на особенностях течения заболевания, в качестве вторичных критериев оценки эффективности использовались шкалы MODS. Для оценки тяжести перитонита в динамике применялся индекс MPI.
В результате оценки первичного критерия эффективности — изменение общего балла по шкале SOFA на 3-й день, по сравнению с исходным значением при поступлении — в популяции всех включенных пациентов (основная популяция для оценки первичного критерия эффективности) среднее изменение оценки по шкале SOFA на 3-й день по сравнению с исходным уровнем составило 1,80 ± 0,91 балла. Аналогичные результаты получены в популяции по протоколу: среднее изменение оценки по шкале SOFA на 3-й день по сравнению с исходным уровнем было равно 1,82 ± 0,89 балла.
При дополнительном анализе изменений параметров на 3-й день по сравнению с исходным уровнем было выявлено, что в группе Реосорбилакта наблюдаются статистически значимое снижение выраженности полиорганной недостаточности и тяжести состояния по таким оцениваемым шкалам, как SOFA, MODS II и MPI, снижение выраженности эндогенной интоксикации, оцениваемой по биохимическим (концентрации креатинина, билирубина) и иммунологическим (количество лейкоцитов, СРБ, соотношение нейтрофилов и лимфоцитов) показателям, а также снижение средних значений температуры и ЧСС.
В группе Реосорбилакта также наблюдались статистически значимые изменения на 3-й день по сравнению с исходным уровнем таких параметров эндогенной интоксикации, как АсАТ, АлАТ, среднемолекулярные олигопептиды, число тромбоцитов, а также снижение ЧД.
Нужно заметить, что уже на 3-й день терапии у участников основной группы выявлено уменьшение процента отклонений некоторых лабораторных показателей функции элиминационных органов (рис. 5).
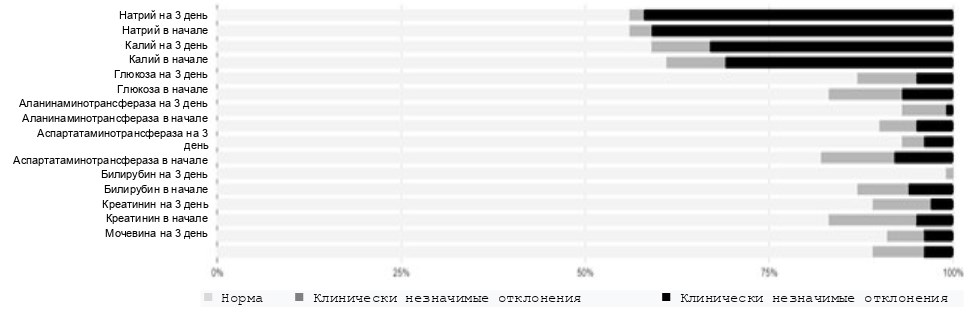 Рис. 5. Процент отклонений показателей функции элиминационных органов, глюкозы и электролитов крови до и после 3-дневного курса лечения Реосорбилактом
Рис. 5. Процент отклонений показателей функции элиминационных органов, глюкозы и электролитов крови до и после 3-дневного курса лечения Реосорбилактом
Норма Клинически незначимые отклонения Клинически значимые отклонения
Натрий на 3-й день Натрий в начале
Калий на 3-й день Калий в начале
Глюкоза на 3-й день Глюкоза в начале
АлАТ на 3-й день АлАТ в начале
АсАТ на 3-й день АсАТ в начале
Билирубин на 3-й день Билирубин в начале
Креатинин на 3-й день Креатинин в начале
Мочевина на 3-й день Мочевина в начале
Таким образом, полученные результаты свидетельствуют о том, что препарат Реосорбилакт эффективно обеспечивает улучшение состояния пациентов, снижение выраженности полиорганной недостаточности, эндогенной интоксикации по большинству оцененных в исследовании показателей у пациентов с гнойным перитонитом.
Заключение
Имеющаяся сегодня доказательная база и современные международные руководства отдают предпочтение сбалансированным кристаллоидным инфузионным растворам как патогенетической терапии генерализованного перитонита и абдоминального сепсиса. Результаты масштабного рандомизированного многоцентрового исследования RheoSTAT-CP0691 по протоколу гнойного перитонита свидетельствуют о том, что Реосорбилакт является эффективным и безопасным препаратом для терапии гнойного перитонита.
Эффективность Реосорбилакт была выражена в статистически значимом улучшении интегральных показателей состояния пациентов по шкалам SOFA, MODS и MPI. Малообъемная инфузионная терапия Реосорбилактом (200–400 мл в сутки) способствует увеличению ОЦК и уменьшению общего объема инфузии, необходимой для достижения терапевтического эффекта, без риска гипергидратации и перегрузки жидкостью, что особенно важно для пациентов в критических состояниях.
Лактат в составе Реосорбилакта (экзогенный) не влияет на уровень эндогенного лактата, что обусловливает высокий профиль безопасности применения раствора. В комплексе интенсивной терапии введение Реосорбилакта способствовало снижению гипертермии, ЧСС и уровня лейкоцитов как проявления эндогенной интоксикации. Применение Реосорбилакта уже за первые 3 дня интенсивной терапии обеспечивало быструю и безопасную нормализацию реологических показателей крови у пациентов с гнойным перитонитом.
Таким образом, Реосорбилакт является эффективным и безопасным средством для терапии пациентов с гнойным перитонитом. Исследование RheoSTAT-CP0691 обосновывает целесообразность применения препарата Реосорбилакт в комплексной терапии гнойного перитонита.
Авторы:
С. Агоп1, В.Х Шарипова2, К. Кашибадзе3, Д. Вашадзе4, В.Тевдорадзе5, И.В. Колосович6, С.Б.Пеев7, А.В. Лигоненко8, В. Кожокару9, А. Белый10
Литература:
- AdesunkanmiA.R.K., OseniS.A., Adejuyigbe O., et al. Acute generalized peritonitis in African children: assessment of severity of illness using modified APACHE II score. ANZ J. Surg. 2003; 73: 275-9.
- Drexel S., Tseng D. Primary peritonitis: an index case of mycoplasma hominis infection in a healthy female. Case Rep. Surg. 2018; 2018: 1-4.
- Ghosh P., Mukherjee R., Sarkar S., et al. Epidemiology of secondary peritonitis: analysis of 545 cases. Int. J. Sci. Stud. 2016; 3: 83-8.
- Ross J.T., Matthay M.A., Harris H.W. Secondary peritonitis: principles of diagnosis and intervention. BMJ. 2018; 361: k1407.
- Strobel O., Werner J., Büchler M. Surgical therapy of peritonitis. Chirurg. 2011; 82: 242-8.
- Sartelli M., Catena F., Ansaloni L., et al. Complicated intra-abdominal infections worldwide: the definitive data of the CIAOW study. World J. Emerg. Surg. 2014; 9: 37.
- Chichom-Mefire A., Fon T., Ngowe-Ngowe M. Which cause of diffuse peritonitis is the deadliest in the tropics? A retrospective analysis of 305 cases from the south-west region of Cameroon. World J. Emerg. Surg. 2016; 11: 14.
- Adesunkanmi A.R.K., Badmus T.A. Pattern of antibiotic therapy and clinical outcome in acute generalized peritonitis in semi-urban and rural Nigerians. Chemotherapy. 2006; 52: 69-72.
- Søreide K., Thorsen K., Søreide J. Strategies to improve the outcome of emergency surgery for perforated peptic ulcer. Br. J. Surg. 2014; 101: e51-64.
- Armstrong C. Updated guideline on diagnosis and treatment of intra-abdominal infections. American Family Physician. 2010 Sep 15; 82 (6).
- Sartelli M., Catena F., Moore E. Management of intra-abdominal infections: recommendations by the WSES 2016 consensus conference. World Journal of Emergency Surgery. 2017; 12: 22.
- Hippensteel J.A., Uchimido R., Tyler P.D., Burke R.C., Han X., Zhang F., et al. Intravenous fluid resuscitation is associated with septic endothelial glycocalyx degradation. Crit. Care. 2019; 23 (259). https://doi.org/10.1186/s13054–019–2534–2.
- Cordemans C., De Laet I., Van Regenmortel N., Schoonheydt K., Dits H., Huber W., et al. Fluid management in critically ill patients: the role of extravascular lung water, abdominal hypertension, capillary leak, and fluid balance. Ann. Intensive Care. 2012; 2: S1.
- Malbrain M.L., Marik P.E., Witters I., Cordemans C., Kirkpatrick A.W., Roberts D.J., et al. Fluid overload, de-resuscitation, and outcomes in critically ill or injured patients: a systematic review with suggestions for clinical practice. Anaesthesiol. Intensive Ther. 2014; 46: 361-80.
- Heung M., Wolfgram D.F., Kommareddi M., Hu Y., Song P.X., Ojo A.O. Fluid overload at initiation of renal replacement therapy is associated with lack of renal recovery in patients with acute kidney injury. Nephrol. Dial. Transplant. 2012; 27: 956-61.
- Bouchard J., Soroko S.B., Chertow G.M., Himmelfarb J., Ikizler T.A., Paganini E.P., et al. Fluid accumulation, survival and recovery of kidney function in critically ill patients with acute kidney injury. Kidney Int. 2009; 76: 422-7.
- Stein A., de Souza L.V., Belettini C.R., Menegazzo W.R., Viégas J.R., Costa Pereira E.M., et al. Fluid overload and changes in serum creatinine after cardiac surgery: predictors of mortality and longer intensive care stay. A prospective cohort study. Crit. Care. 2012; 16: R99.
- Best M.W., Jabaley C.S. Fluid management in septic shock: a review of physiology, goal-directed therapy, fluid dose, and selection. Curr. Anesthesiol. Rep. 2019; 9: 151-157. https://doi.org/10.1007/s40140-019-00330-3.
- Marik P., Bellomo R. A rational approach to fluid therapy in sepsis. Br. J. Anaesth. 2016; 116 (3): 339.
- Hahn R., Lyons G. The half-life of infusion fluids: an educational review. Eur. J. Anaesthesiol. 2016; 33 (7): 475-82.
- Caironi P., Tognoni G., Masson S., Fumagalli R., Pesenti A., Romero M., et al. Albumin replacement in patients with severe sepsis or septic shock. N. Engl. J. Med. 2014; 370 (15): 1412-21.
- Finfer S., Bellomo R., Boyce N., French J., Myburgh J., Norton R., et al. A comparison of albumin and saline for fluid resuscitation in the intensive care unit. N. Engl. J. Med. 2004; 350 (22): 2247-56.
- SAFE Study Investigators; Australian and New Zealand Intensive Care Society Clinical Trials Group; Australian Red Cross Blood Service; George Institute for International Health, Myburgh J., Cooper D., Finfer S., Bellomo R., Norton R., Bishop N., Kai Lo S., Vallance S. Saline or albumin for fluid resuscitation in patients with traumatic brain injury. N. Engl. J. Med. 2007 Aug 30; 357 (9): 874-84. doi: 10.1056/NEJMoa067514.
- Myburgh J.A., Finfer S., Bellomo R., Billot L., Cass A., Gattas D., et al. Hydroxyethyl starch or saline for fluid resuscitation in intensive care. N. Engl. J. Med. 2012; 367 (20): 1901-11.
- Perner A., Haase N., Guttormsen A., Tenhunen J., Klemenzson G., Åneman A., et al. Hydroxyethyl starch 130/0.42 versus Ringer’s acetate in severe sepsis. N. Engl. J. Med. 2012; 367 (2): 124-34.
- Rhodes A., Evans L.E., Alhazzani W., Levy M.M., Antonelli M., Ferrer R., et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock: 2016. Crit. Care Med. 2017; 45 (3): 486-552.
- MacDonald N., Pearse R. Are we close to the ideal intravenous fluid? Br. J. Anaesth. 2017; 119 (suppl. 1): i63-71.
- Magee C.A., Bastin M.L.T., Laine M.E., Bissell B.D., Howington G.T., Moran P.R., et al. Insidious harm of medication diluents as a contributor to cumulative volume and hyperchloremia: a prospective, open-label, sequential period pilot study. Crit. Care Med. 2018; 46 (8): 1217-23.
- Self W.H., Semler M.W., Wanderer J.P., Wang L., Byrne D.W., Collins S.P., et al. Balanced crystalloids versus saline in noncritically ill adults. N. Engl. J. Med. 2018; 378 (9): 819-28.
- Semler M.W., Self W.H., Wanderer J.P., Ehrenfeld J.M., Wang L., Byrne D.W., et al. Balanced crystalloids versus saline in critically ill adults. N. Engl. J. Med. 2018; 378 (9): 829-39.
- Dalton C. Why did sterile salt water become the IV fluid of choice? NPR. 2018. Available at: https://www.npr.org/sections/health-shots/2018/03/31/597666140/why-did-sterile-salt-water-become-the-iv-fluid-of-choice. Accessed: 02/04/2018.
- Кондрацкий Б., Новак В. Опыт применения в клинической практике комплексного инфузионного препарата Реосорбилакта. Искусство лечения. 2006; № 1: с. 34–36.
- Хамидов Д.Б., Косимов З.К., Хомидов Д.Д., Киямов С.Э. Комплексный полифункциональный раствор Реосорбилакт в интенсивной терапии эндогенной интоксикации у больных острым перитонитом. Научно-практический журнал ТИППМК. 2011; № 2: с. 77–79.
- Алиев Н.А., Бобиев А.Б., Хамидов Д.Б., Баротов Э.Д., Буриев Т.Н., Курбанов Д.А. и др. Реосорбилакт и Латрен в коррекции эндогенной интоксикации и оксидантного стресса у больных острым деструктивным панкреатитом. Медицина неотложных состояний. 2015; том 64, № 1: с. 57–59.
- Проничев В., Стяжкина С., Михайлов А. Эффективность лечения Реосорбилактом пациентов с синдромом диабетической стопы. Здоровье, демография, экология финно-угорских народов. 2016; № 2: с. 30–32.
- Рижко О.О. Инфузионная терапия Реосорбилактом. Укр. пульмонологический журнал. 2002; № 1: с. 94–96.