Особливості управління болем у вагітних та породіль
Мета – оцінити ефективність і несприятливі побічні ефекти (якщо такі є) внутрішньовенної інфузії 1000 мг парацетамолу як методу полегшення болю породіллям під час активної фази пологів та в післяопераційному періоді після кесаревого розтину.
Матеріали та методи. Досліджено 43 вагітні жінки в І періоді пологів з активною пологовою діяльністю. Критерії вибору: здорові першонароджені породіллі низького ризику, що вперше народжували, віком 18–35 років; спонтанний початок пологів у терміні 37–40 тижнів вагітності; перший період пологів із розкриттям шийки матки на 3–5 см; один живий плід; головне передлежання. Препаратом парацетамолу обрано Інфулган розчин д/інф. 10 мг/мл по 100 мл. Показник інтенсивності болю визначено за візуально-аналоговою шкалою (ВАШ) – метод суб’єктивної оцінки болю. Пацієнтка відмічала на неградуйованій лінійці довжиною 10 см точку, яка відповідає ступеню вираженості болю.
Під час оцінювання динаміки, зміни інтенсивності болю вважали об’єктивними й істотними, якщо справжнє значення ВАШ відрізнялося від попереднього більше ніж на 1,3 см. Групу порівняння склали 20 вагітних у І періоді пологів, яким не проводилось знеболення за власним бажанням. Також проводилось дослідження ефективності комплексної мультимодальної анестезії (Інфулган (парацетамол) та Кейдекс (декскетопрофен)) у 5 (11,6%) породіль після розродження шляхом кесаревого розтину.
Результати. Використання внутрішньовенної ін’єкції парацетамолу для знеболювання під час пологів є ефективною аналгезією. Відмічено початкове, але значуще зниження оцінки ВАШ через 30 хвилин після введення Інфулгану та статистично значуще зменшення болю через 2, 3 і 4 години порівняно з оцінкою болю за ВАШ до лікування. У групі жінок, яким не проводили знеболювання, інтенсивність больового синдрому невпинно зростала.
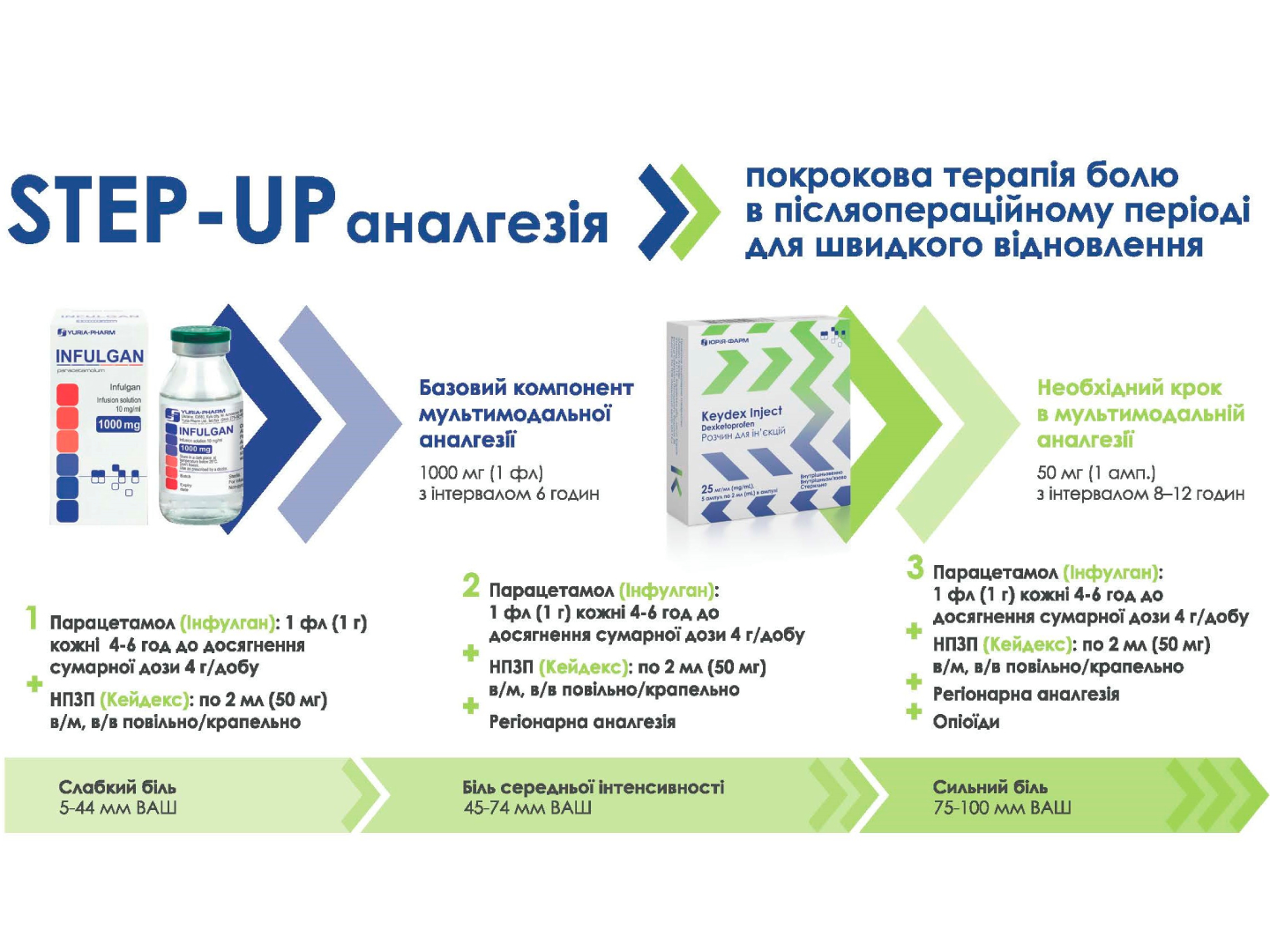
У післяопераційному періоді, після кесаревого розтину, жінкам проводили комбіноване знеболювання із застосуванням Інфулгану (парацетамол) як базового компонента мультимодальної аналгезії та Кейдексу (декскетопрофен) як необхідного кроку мультимодального знеболювання. Вищезазначена комбінація препаратів дала змогу проводити Step-Up-аналгезію – покрокову терапію болю. Інфулган призначали по 1 флакону (1000 мг) кожні 6 годин внутрішньовенного введення, Кейдекс – по 1 ампулі кожні 8 годин внутрішньом’язово. Додавання до аналгезії Кейдексу (декскетопрофену) забезпечило адекватний ефект знеболювання і не потребувало введення опіоїдних анальгетиків у післяопераційному періоді.
Висновки. Парацетамол для внутрішньовенного введення є ефективним неопіоїдним препаратом для полегшення болю при пологах без будь-яких істотних побічних ефектів для матері та плода. Відсутність будь-яких побічних ефектів у матері (седація, пригнічення дихання, затримка випорожнення шлунка, нудота та блювання) або неонатальних побічних ефектів (пригнічення дихання та зниження балів за шкалою Апгар), пов’язаних з опіоїдами, дозволяє рекомендувати Інфулган для полегшення болю при пологах.
Покрокова терапія болю Step-Up у післяопераційному періоді дає змогу зменшити дозування кожного з анальгетиків та частоту й прояви побічної дії препаратів. Застосування Інфулгану та Кейдексу, як методу управління болем шляхом Step-Up-аналгезії в післяопераційному періоді в породіль, має високу ефективність, належну переносимість і задоволеність пацієнток.
Дослідження виконано відповідно до принципів Гельсінської декларації. Протокол дослідження ухвалено Локальним етичним комітетом зазначеної в роботі установи. На проведення досліджень отримано інформовану згоду жінок. Автори заявляють про відсутність конфлікту інтересів.
Ключові слова: знеболювання пологів, мультимодальна анестезія, неопіоїдні анальгетики, породіллі.
Стаття. На сьогодні встановлено, що інтенсивність болю, яку відчувають породіллі, впливає на хід пологів, стан плода та психо-емоційне самопочуття матері. При виборі методу управління болем у жінок слід зважати на можливі непрогнозовані зміни гемодинаміки та метаболізму у відповідь на оперативні втручання (кесарів розтин), а також на високу чутливість до анестетиків [1,2].
Необхідно ретельно зважувати показання до будь-якого інвазивного втручання у всіх пацієнтів, а особливо в групі пацієнтів з коморбідністю, беручи до уваги потенційну дестабілізацію структурно-функціональної цілісності організму та розвиток декомпенсації серцево-судинної системи з результатом поліорганної дисфункції [3].
Народження дитини пов’язано із значними больовими відчуттями для більшості жінок. Біль під час пологів – це складне, суб’єктивне та багатогранне фізіологічне явище, яке різниться за інтенсивністю серед жінок і піддається багатьом соціальним і культурним модифікаторам. Він охоплює як сенсорний компонент, так і дуже важливі емоційні, мотиваційні та когнітивні аспекти [4]. Особливо під час першого періоду пологів больові відчуття викликають генералізовану нейроендокринну стресову реакцію, викликаючи помітні фізіологічні зміни в показниках споживання кисню, функціонування серцево-судинної та дихальної системи, а також інтенсивності перейм [ 5 ] .
Таким чином, для сучасного акушера стає обов’язковим забезпечити адекватне знеболювання породіль.
При виборі методу управління болем при оперативному розродженні та в післяопераційному періоді, при самостійних пологах та знеболенні ускладнень пологів через природні пологові шляхи (глибокі розриви піхви, епізіотомія, розриви промежини) основним критерієм є безпека матері та плоду [6].
Ідеальний анальгетик для пологів повинен мати потужну анальгетичну ефективність із незначними побічними ефектами, щоб використовувати його для полегшення болю. Системні опіоїди широко використовуються для анальгезії пологів, але їх використання пов’язано з побічними ефектами матері (дисфорія, седативний ефект, пригнічення дихання, нудота та блювання та затримка спорожнення шлунка) і плода (дистрес , рання неонатальна респіраторна депресія та проблеми з поведінкою та годуванням) протягом шести тижнів після пологів [ 7 ]. Вище зазначене призвело до необхідності використання альтернативного безопіоїдного підходу для знеболення вагітної під час пологів.
Парацетамол є ефективним ненаркотичним анальгетиком високим профілем безпеки в добовому дозуванні до 4 г [ 8 ].
Вважається, що парацетамол чинить анальгетичний ефект шляхом пригнічення синтезу простагландинів в центральній нервовій системі (центральна дія) і блоку генерації больового імпульсу на периферії [ 9 ].
Крім того, він має серотонінергічний (5-НТ) механізм і механізм канабіноїдного агонізму, що сприяє його знеболювальному ефекту. У порівнянні з іншими опіоїдами та нестероїдними протизапальними препаратами, парацетамол має сприятливий профіль безпеки без будь-якого ризику вроджених аномалій [ 10 ]. Використання внутрішньовенного шляху введення парацетамолу для полегшення болю під час пологів є перевагою завдяки покращеній біодоступності та ранньому початку дії з вищою середньою максимальною концентрацією препарату в плазмі та більш раннім часом досягнення максимальної концентрації.
На сьогодні є наукові праці щодо вивчення ролі парацетамолу у превентивному підході до лікування післяопераційного болю [ 11, 12 ] , але залишається важливим подальше дослідження переваг і недоліків використання парацетамолу як інтранатального анальгетика.
Таким чином, метою поточного дослідження було оцінити ефективність і несприятливі побічні ефекти (якщо такі є) внутрішньовенної інфузії 1000 мг парацетамолу під час активної фази пологів як методу полегшення болю породіллям.
Матеріали та методи дослідження. Було досліджено 43 вагітні жінки в І періоді пологів із активною пологовою діяльністю. Критеріями вибору були здорові першонароджені породіллі низького ризику; віком 18–35 років; із спонтанним початком пологів в терміні 37–40 тижнів вагітності; перший період пологів з розкриттям шийки матки на 3–5 см; один живий плід; головне передлежання. Препаратом парацетамолу обрали Інфулган розчин д/інф. 10 мг/мл по 100 мл.
Показник інтенсивності болю визначали за шкалою ВАШ. Візуально-аналогова шкала (ВАШ) – метод суб’єктивної оцінки болю. Пацієнтка відмічала на неградуйованій лінійці довжиною 10 см точку, яка відповідає ступеню вираженості болю. Ліва межа лінійки відповідає визначенню «болю немає», права – «найгірший біль, який можна собі уявити». Як правило, використовують паперову, картонну або пластмасову лінійку довжиною 10 см. Зі зворотного боку лінійки нанесено сантиметрові поділки, за якими фіксувалось отримане значення в цифрах. При динамічній оцінці зміни інтенсивності болю вважають об’єктивними й істотними, якщо справжнє значення ВАШ відрізняється від попереднього більше ніж на 1,3 см.

Основним оцінюваним результатом була ефективність Інфулгану для забезпечення достатньої кількості аналгезії, що вимірювалося зміною оцінки інтенсивності болю за візуальною аналоговою шкалою (ВАШ) у різні періоди часу після введення препарату.
Породілля описувала інтенсивність болю за шкалою ВАШ, безпосередньо перед введенням Інфулгану та в подальшому через 30 хвилин, 1 годину, 2 години, 3 години та 4 години після введення.
Результати дослідження
Результати цього дослідження чітко демонструють, що використання внутрішньовенної ін’єкції парацетамолу для знеболення під час пологів є ефективною аналгезією (див. табл.). За даними таблиці спостерігається початкове, але значуще зниженням оцінки ВАШ через 30 хвилин після введення Інфулгану та статистично значущим зменшенням болю через 2 ,3 і 4 години, порівняно з оцінкою болю за ВАШ до лікування.
В групі жінок, яким не проводилось знеболення , інтенсивність больового синдрому невпинно зростала.
Високі показники інтенсивності болю перед початком анальгезії можна пояснити залученням жінок з активною пологовою діяльністю що потребувало інтенсивного знеболення.
Жодних негативних ефектів для матері чи новонародженого в групі проведення анальгезії не спостерігалося. Також, не було відмінностей у виникненні дистресу плода під час пологів або знижених неонатальних балів за шкалою Апгар.
Таблиця
Оцінка болю за ВАШ в залежності від знеболення пологів
|
Оцінка болю за шкалою VAS |
Показник ВАШ в групі жінок, які отримували знеболення пологів Інфулганом |
Показник ВАШ в групі жінок, які не отримували знеболення |
|
Перед в/в введенням |
6,91+1,31 |
7,02+1,28 |
|
Через 30 хв |
6,18+1,02* |
6,90+1,09 |
|
Через I годину |
5,12±1,02** |
6,72+1,12 |
|
Через 2 години |
4,76+1,04*** |
6,86+1,04 |
|
Через 3 години |
5,36+1,05 **** |
7,23+1,21 |
|
Через 4 години |
6,51+ 1,10 |
7,20+1,15 |
Примітка:
*достовірність різниці між показниками в групах;
** – достовірність різниці між показниками в межах одної групи через 1 годину порівняно із вихідним показником;
*** – достовірність різниці між показниками в межах одної групи через 2 години порівняно із вихідним показником;
**** – достовірність різниці між показниками в межах одної групи через 3 години порівняно із вихідним показником
Важливим залишається актуальність контролю післяопераційного больового синдрому. Виражений больовий синдром негативно впливає на післяпологовий період. Від того на скільки ми можемо контролювати ступінь больового синдрому, залежить термін перебування породіллі у стаціонарі, розвиток ускладнень, особливо у жінок групи високого ризику, якість реабілітації, розвиток синдрому хронічного болю та частота післяпологової депресії.
Немає «ідеального» анальгетика чи метода лікування гострого больового синдрому. Але максимально наблизитись до рішення даної проблеми нам дозволяє комплексний підхід, який включає в себе декілька факторів: професійний сестринське спостереження, поєднання фармакологічних та не фармакологічних методів знеболення, збалансована(мультимодальна) аналгезія з індивідуальним підбором доз, технік, режимів введення анальгетиків.
Теоретичні підходи до зменшення деструктивних впливів стресу, пов’язаного як із наявністю основного захворювання, так і з хірургічною травмою, беруть свій початок у 20-х роках минулого століття. На основі досліджень Н. Kehlet розвинулася одна з найголовніших складових сучасної анестезіології – мультимодальна програма FTS (Fast Track Surgery – «хірургія швидкого відновлення») або ERAS (Enhanced Recovery After Surgery – «прискорене одужання після хірургічного втручання»). Ці програми охоплюють питання передопераційної підготовки, особливостей оперативної техніки та ведення пацієнтів в післяопераційному періоді. Вона спрямована як на зниження відповіді організму на стрес внаслідок хірургічного втручання та болю, так і на прискорення одужання та скорочення терміну перебування хворого у стаціонарі.
Основною метою програми ERAS є позитивний вплив на три ключові речі, що перешкоджають швидкому відновленню організму пацієнта: постійну необхідність парентерального знеболювання; дисфункцію травної системи (як реакцію на оперативне втручання і як побічний ефект медикаментозної терапії); довготривалу іммобілізацію як результат післяопераційного болю.
Шляхами подолання зазначених негативних наслідків хірургічного втручання згідно програми ERAS вважають: модифіковану передопераційну підготовку, зменшення хірургічної травми під час операції (мініінвазивне втручання – це менша хірургічна травма, а отже, менша больова імпульсація в ранньому післяопераційному періоді), подолання інсулінорезистентності в ранньому післяопераційному періоді; проведення мультимодальної аналгезії, яка передбачає застосування різних технік аналгезії та різних груп лікарських препаратів; попередження інтраопераційної гіпотермії; оптимізація перед – та інтраопераційної інфузії; передопераційна вуглеводна дієта; раннє ентеральне харчування [13].
Основною складовою мультимодальної аналгезії є одночасне призначення двох і більше аналгетиків і/або використання декількох методів знеболювання, які мають різні механізми дії, що дає змогу досягти адекватної аналгезії з мінімумом побічних ефектів.
Принцип мультимодальної аналгезії заснований на припущенні, що одночасне використання в основному не опіатних анальгетиків можуть потенціювати дію один одного, що викликає в свою чергу адекватний рівень знеболення при зниженні пов’язаних з опіоїдами побічних ефектів. Зниження використання опіоїдів та мінімізація їх побічної дії є ключовими компонентами стандартного анальгетичного протоколу ERAS [14].
Дані сучасних досліджень доводять, що парацетамол за умови внутрішньовенного введення (Інфулган) чинить опіоїдзберігаючий ефект, а в разі порівнювання знеболюючої дії парацетамолу окремо або в комбінації з іншими НПЗЗ повідомлялося про підвищення ефективності аналгезії при комбінації двох препаратів, ніж при окремому застосуванні кожного з них [15,16].
Серед 43 досліджених нами жінок, яким проводилось знеболення в І періоді за допомогою препарату Інфулган, 5 пацієнток (11,6%) було розроджено шляхом кесаревого розтину за акушерськими показаннями.
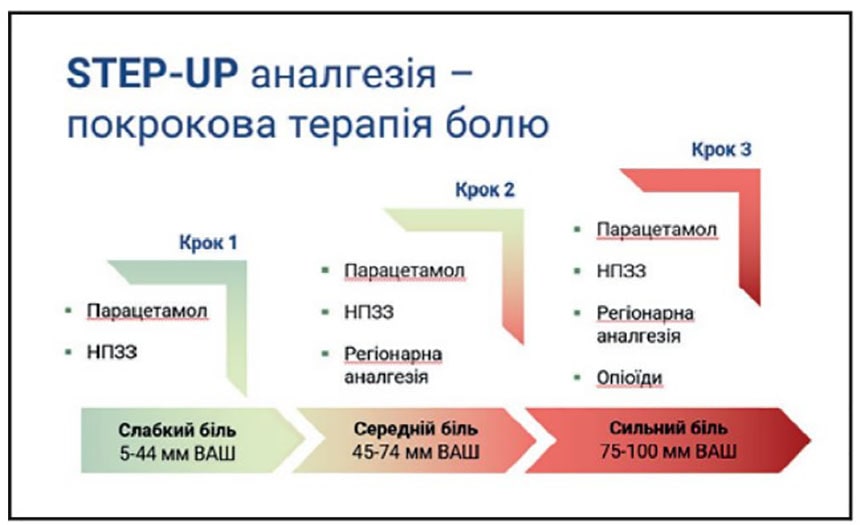
В післяопераційному періоді їм проводилось комбіноване знеболення із застосуванням препаратів Інфулган (парацетамол) в якості базового компонента мультимодальної аналгезії та Кейдекс (декскетопрофен) – необхідного кроку мультимодального знеболення. Вище зазначена комбінація препаратів дозволяє провести Step-Up аналгезію – покрокову терапію болю. Інфулган призначали по 1 флакону ( 1000 мг) кожні 6 годин в\в введення та Кейдекс по 1 ампулі кожні 8 годин внутрішньом’язево.
Покрокова терапія болю Step-Up дозволяє зменшити дози кожного з анальгетиків, підвищити антиноцицептивний потенціал, зменшити частоту та прояви побічної дії препаратів. Додавання до аналгезії Кейдекс (декскетопрофену) дозволило отримати адекватний ефект знеболення і не потребувало введення опіоїдних анальгетиків в післяопераційному періоді [17].
Важливим є той факт, що планове знеболення Інфулганом по графіку протягом доби зменшує частоту екстреної аналгезії, в порівнянні зі знеболенням «за вимогою» пацієнтки [18].
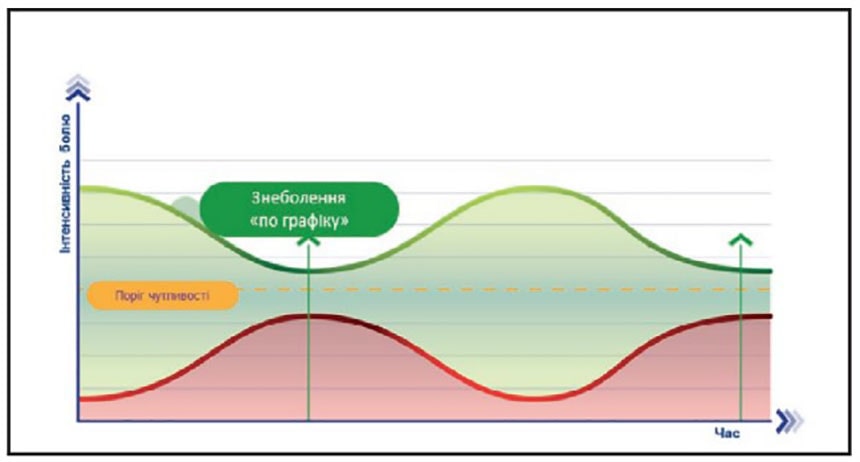
Післяопераційне планове знеболення по графіку (Around-the-clock administration) підтримує концентрацію аналгетика для знеболення протягом доби, знижує рівень болю за шкалою ВАШ, знижує частоту екстренної аналгезії [Shogo Inoue, Hirotsugu Miyoshi, Tetsutaro Hayashi/Postoperative around-the-clock administration of intravenous acetaminophen for pain control following robot-assisted radical prostatectomy/ Scientific Reports March 2021/Scientific Reports 11(1)].
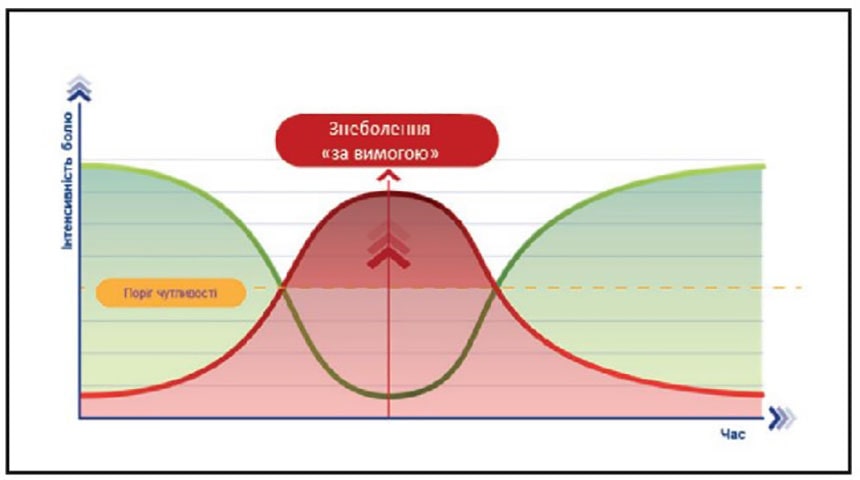
Застосування Інфулгану та Кейдексу, як методу управління болем шляхом Step-Up аналгезії в післяопераційному періоді у породіль виявило високу ефективність, належну переносимість та задоволеність пацієнток.
Відомості про авторів:
- Давидова Юлія Володимирівна – д.мед.н., магістр державного управління, зав. відділення акушерських проблем екстрагенітальної патології, ДУ «ІПАГ імені акад. О.М. Лук’янової НАМН України».
- Мар’ясова Ольга Володимирівна – лікар анестезіолог-реаніматолог, зав. відділенням анестезіології з ліжками інтенсивної терапії та реанімації для вагітних, ДУ «ІПАГ імені акад. О.М. Лук’янової НАМН України».
- Лиманська Аліса Юріївна – канд.мед.наук, пров.н.с. відділення акушерських проблем екстрагенітальної патології ДУ «ІПАГ імені академіка О.М. Лук’янової, НАМН України»; доц. каф. внутрішньої медицини № 2 НМУ імені О.О. Богомольця.
- Кравець Ольга Михайлівна – лікар акушер-гінеколог ДУ «ІПАГ імені академіка О.М. Лук’янової НАМН України».
Висновки:
Парацетамол для внутрішньовенного введення є ефективним неопіоїдним препаратом для полегшення болю при пологах без будь-яких істотних побічних ефектів для матері та плода. Відсутність будь-яких побічних ефектів у матері (седація, пригнічення дихання, затримка випорожнення шлунка, нудота та блювота) або неонатальних побічних ефектів (пригнічення дихання та зниження балів за шкалою Апгар), пов’язаних із опіоїдами дозволяє рекомендувати Інфулган для полегшення болю при пологах. Покрокова терапія болю Step-Up в післяопераційному періоді дозволяє зменшити дози кожного з анальгетиків та зменшити частоту та прояви побічної дії препаратів. Застосування Інфулгану та Кейдексу, як методу управління болем шляхом Step-Up аналгезії в післяопераційному періоді у породіль виявило високу ефективність, належну переносимість та задоволеність пацієнток.
Література:
- Graham GG, Scott KF, Day RO. Tolerability of paracetamol. Drug Saf. 2005;28(3):227–40.
- Smith HS. Potential analgesic mechanisms of acetaminophen. Pain Physician. 2009;12(1):269–80.
- American College of Obstetricians and Gynecologists’ Presidential Task Force on Pregnancy and Heart Disease and Committee on Practice Bulletins–Obstetrics. ACOG Practice Bulletin No. 212: Pregnancy and Heart Disease. Obstet Gynecol. 2019 May. 133 (5):e320-e356.
- Lowe NK. The nature of labour pain. American Obstetric Gynaecology. 2002;186(5):S16–S24.
- Pandya ST. Labour analgesia: Recent advances. Indian Journal of Anaesthesiology. 2010;54(5):400–08.
- Ong C. K., Seymour R. A., Lirk P., Merry A.F. Combining paracetamol (acetaminophen) with nonsteroidal antiinflammatory drugs: a qualitative systematic review of analgesic efficacy for acute postoperative pain. Anesth Analg. 2010;110(4):1170–1179.
- Makkar JK, Jain K, Bhatia N, Jain V, Mithrawal SM. Comparison of analgesic efficacy of paracetamol and tramadol for pain relief in active labour. Journal of Clinical Anesthesia. 2015;27:159–63.
- Smith HS. Potential analgesic mechanisms of acetaminophen. Pain Physician. 2009;12(1):269–80.
- Aronoff DM, Oates JA, Boutaud O, Arbor A. New insights into the mechanism of action of acetaminophen: Its clinical pharmacologic characteristics reflect its inhibition of the two prostaglandin H2 synthases. Clinical Pharmacology and Therapeutics. 2006;79(1):9–19.
- Smith HS. Potential analgesic mechanisms of acetaminophen. Pain Physician. 2009;12(1):269–80.
- Stoudenmire LG, Norman CM, Latif EZ. Impact of postoperative intravenous acetaminophen on opioid requirements and pain scores following gynaecologic procedures. J Pharm Pract. 2015:pii. 0897190014568384
- Soltani G, Molkizadeh A, Amini S. Effect of intravenous acetaminophen (paracetamol) on hemodynamic parameters following endotracheal tube intubation and postoperative pain in caesarean section surgeries. Anesth Pain Med. 2015;5(6):e30062.
- Nilsson U., Gruen R., Myles P.S. Postoperative recovery: the importance of the team. Anaesthesia. 2020;75(S1):e158–64.
- Cuomo A, Bimonte S, Forte CA, Botti G, Cascella M. Multimodal approaches and tailored therapies for pain management: the trolley analgesic model. J Pain Res. 2019;12:711-714.
- Nilsson U., Gruen R., Myles P.S. Postoperative recovery: the importance of the team. Anaesthesia. 2020;75(S1):e158–64.
- Ong C. K., Seymour R. A., Lirk P., Merry A.F. Combining paracetamol (acetaminophen) with nonsteroidal antiinflammatory drugs: a qualitative systematic review of analgesic efficacy for acute postoperative pain. Anesth Analg. 2010;110(4):1170–1179.
- Luc Martinez, Evan Ekman, Nardine Nakhla/Perioperative Opioid-sparing Strategies: Utility of Conventional NSAIDs in Adults/Clin Ther . 2019 Dec;41(12):2612-2628. doi: 10.1016/j.clinthera.2019.10.002.
- Shogo Inoue, Hirotsugu Miyoshi, Tetsutaro Hayashi/Postoperative around-the-clock administration of intravenous acetaminophen for pain control following robot-assisted radical prostatectomy/Scientific Reports March 2021/Scientific Reports 11(1)